Учитывая отраслевые сырьевые особенности, в качестве основного компонента питательных сред может быть использовано зерновое, виноградное, плодово-ягодное или мелассовое сусло. Однако наиболее универсальным и сбалансированным следует признать солодовое неохмеленное сусло с содержанием 8–10% СВ.
Для приготовления сусла в лаборатории используют ячменный солод крупного помола с высокой осахаривающей способностью. В 1 л воды вносят 250 г солода и нагревают до 50°С. Через 30 мин температуру повышают до 55°С, а еще через 30 мин постепенно поднимают до 62,5–63°С. При этой температуре выдерживают до исчезновения реакции на крахмал (йодная проба).
Полученное сусло отделяют от дробины путем фильтрации через марлю и вату, разбавляют водой до нужной концентрации, разливают по колбам и стерилизуют при 112°С 30 мин. Если рН ниже 5,5, то сусло подщелачивают 10%-ным раствором соды или едкого кали до получения рН 5,6–6,0. Полученное таким образом сусло желательно очистить от примесей кизельгуром или отстаиванием в холодильнике и фильтрацией через бумажный фильтр.
В отсутствие солодового вполне применимо зерновое сусло, осахаренное комплексом ферментных препаратов с обязательным внесением дрожжевой золки и 0,3–0,5% дрожжевого автолизата перед автоклавированием[1].
Для приготовления жидкой питательной среды осахаренное и отфильтрованное сусло разливают в колбы или пробирки на 1/2–3/4 объема, закрывают ватно-марлевыми пробками и автоклавируют 20 мин при 0,1 МПа.
Густую мелассу отвешивают на технических весах в количестве 200–300 г, смешивают с водой в соотношении 1:3 и нагревают до 75°С, затем насыпают 4% суперфосфата и повышают температуру до 85°С при постоянном помешивании. 33%-ный раствор едкой щелочи в количестве 0,8% по объему к исходной мелассе разводят в 30–50 см3 воды, добавляют к нагретой мелассе и хорошо перемешивают. В результате происходит выпадение осадка трикальцийфосфата, который увлекает за собой коллоиды мелассы и более крупные частицы, осадок быстро оседает на дно, и меласса осветляется. После этого к мелассе добавляют 2,5% сернокислого аммония и 2% суперфосфата в виде вытяжки (1 г суперфосфата и 10 см3 воды нагревают до кипения и фильтруют через бумажный фильтр). Мелассу перемешивают с питательными солями и фильтруют через бумажный фильтр, лучше под вакуумом на воронке Бюхнера.
Осветленную мелассовую среду разводят водой до требуемой концентрации 5–8% СВ по сахарометру и разливают в колбы, пробирки или бутылки; для приготовления твердых питательных сред добавляют агар.
Мелассовое сусло стерилизуют в автоклаве при избыточном давлении 0,05 МПа 30 мин или в аппарате Коха при 100°С в течение 1 ч трое суток подряд.
В химическом стакане в сусло (8–10% СВ) внести необходимое количество агар-агара (2,5 г на 100 см3) и выдержать 10–15 мин, не перемешивая до полного его увлажнения. Стакан поставить на слабый огонь и, постоянно перемешивая, довести до кипения. Содержимое стакана перелить в колбу до 1/2 объема, закрыть ее ватно-марлевой пробкой и автоклавировать 20 мин при 0,1 МПа.
Если питательная среда не требует внесения каких-либо термолабильных ингредиентов, то ее можно сразу после автоклавирования разливать в заранее приготовленные стерильные высушенные чашки Петри. Если же предполагается внесение антибиотиков, факторов роста или других чувствительных к температуре компонентов, то среду в колбе необходимо остудить до 40–45°С, стерильно внести нужные компоненты, перемешать и разливать в чашки Петри. При этом желательно избегать образования комков для получения ровной поверхности питательной среды в чашках. После этого чашки со средой не следует более перемещать, пока агар полностью не остынет.***
Чтобы удалить образовавшийся конденсат и уменьшить его дальнейшее образование, чашки необходимо подсушить. Для этого чашки с агаром переворачиваются крышкой вниз, дно чашки с агаром извлекается и ставится на ребро крышки. В таком положении в боксе под УФ-лампой чашки выдерживаются ≈60 мин. Высушенные чашки закрываются и могут использоваться для работы либо храниться в холодильнике завернутыми в полиэтиленовый пакет, чтобы исключить пересыхание или случайное обсеменение среды. Чашки, хранившиеся в холодильнике, перед работой следует некоторое время выдержать при комнатной температуре или в термостате.
Для приготовления скошенного сусло-агара доведенную до кипения среду (см. пп. 6.1.3) разливают в пробирки до 1/3 ее объема, закрывают ватно-марлевыми пробками и автоклавируют 20 мин при 0,1 МПа. По окончании стерилизации пробирки с горячей средой раскладывают на наклонной поверхности для образования скоса нужной высоты и дают полностью застыть. Остывшие пробирки переносят в штатив и используют по назначению.
В химическом стакане в сусло (8–10% СВ) внести необходимое количество агар-агара (0,5 г/100 см3) и выдержать 10–15 мин, не перемешивая до полного его увлажнения. Стакан поставить на слабый огонь и, постоянно перемешивая, довести до кипения. Содержимое стакана разлить в пробирки до 1/3–1/2 объема, закрыть ватно-марлевыми пробками и автоклавировать 20 мин при 0,1 МПа.
По окончании стерилизации пробирки раскладывают вертикально в штатив и после полного их охлаждения используют по назначению.
6.1.6. АЦЕТАТНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ПОСТОРОННИХ ДРОЖЖЕЙ
На 1000 см3 водопроводной воды берут 10 г уксуснокислого натрия, 10 г хлористого аммония и 5 г глюкозы.
Дрожжевой автолизат добавляют в среду в количестве 3 см3.
Среду разливают в пробирки по 5 см3 и стерилизуют в автоклаве при избыточном давлении 0,05 МПа в течение 30 мин.
6.1.7. СРЕДА С МОНОЙОДУКСУСНОЙ КИСЛОТОЙ
2%-ный сусло-агар после автоклавирования охлаждают до 50°С. В остывшую среду асептически вносят рабочий раствор монойодуксусной кислоты до концентрации 2,5% (97,5 см3 + 2,5 см3 кислоты). Приготовленную среду тщательно перемешивают и разливают в чашки Петри. Конечная рН 5,8.
Посевы исследуемых проб инкубируют не менее 120 ч при 28–30°С.
На данной среде растут дрожжи, не относящиеся к роду Saccharomyces.
Рабочий раствор. В предварительно проавтоклавированную воду внести монойодуксусной кислоты в количестве 7,44 мг на 1,0 см3.
К солодовому суслу концентрацией 8–10% СВ прибавляют 15% желатина и через
30–40 мин, когда желатин набухнет, среду подогревают до 40–50°С, фильтруют через ватво-марлевый фильтр и разливают в пробирки или колбы.
Стерилизуют в аппарате Коха при 100°С по 30 мин трое суток подряд.
6.1.9. СРЕДА САБУРО ДЛЯ ВЫРАЩИВАНИЯ ДРОЖЖЕЙ
К 100 см3 стерильной дрожжевой воды добавляют 5 г пептона, 4 г глюкозы, 1,8 г агара. После того как агар расплавится при нагревании, среду фильтруют и разливают в пробирки.
Стерилизуют 20 мин при избыточном давлении 0,05 МПа или в аппарате Коха дробной стерилизацией.
6.1.10. СИНТЕТИЧЕСКАЯ СРЕДА С ЛИЗИНОМ
Рецептура синтетической среды с лизином следующая.
Глюкоза............................................................ 50 г
Лизин.................................................................. 3 г
KH2PO4................................................................ 1 г
MgSO4................................................................. 1 г
FeSO4............................................................. следы
Каждый компонент среды растворяют в воде отдельно, смешивают в указанном порядке и доводят водопроводной водой до 1000 см3.
В полученную жидкую синтетическую среду вносят агар (2,5%), расплавляют и разливают в пробирки по 10 см3. Среду стерилизуют 20 мин при давлении 0,05 МПа.
После автоклавирования пробирки ставят в штатив для получения скошенной среды.
6.1.11. СРЕДА 10 ДЛЯ ВЫЯВЛЕНИЯ И ПОДСЧЕТА
ЛАКТОБАКТЕРИЙ И ЛЕЙКОНОСТОКА
На 1000 см3 неохмеленного солодового сусла (8% СВ) или 1000 см3 дрожжевой воды добавляют 0,05 г MnSO4·4H2O, по 0,2 г MgSО4·7H2О, цистина или цистеина, Kh2po4, цитрата аммония, 2,5 г ацетата натрия, 20 г сахарозы, 10 г пептона и 50 см3 дрожжевого автолизата.
Каждый компонент среды растворяют в указанном порядке в солодовом сусле (для выращивания лактобактерий) или дрожжевой воде (для выращивания лейконостока). В первом случае рН среды 5,5, во втором – 6,0.
Растворив все компоненты и нормализовав рН, добавляют 2,5% агара и стерилизуют троекратно текучим паром.
Перед использованием в расплавленную среду добавляют стерильный мел (3% к объему среды), тщательно перемешивают и разливают в чашки Петри.
6.1.12. МОЛОЧНЫЙ АГАР БОГДАНОВА
Используется в качестве среды для выявления и учета гнилостных бактерий.
Обезжиренное молоко разливают в пробирки по 5 см3 и троекратно стерилизуют текучим паром либо 20 мин при 0,05 МПа. Отдельно готовят 5%-ный водный агар, разливают его в пробирки по 4–5 см3 и стерилизуют 30 мин при давлении 0,1 МПа.
Перед посевом водный агар расплавляют, соединяют с молоком, и смесь выливают в чашки Петри, куда предварительно была внесена исследуемая проба.
Сусло помещают в колбу и нагревают до кипения в кипятильнике Коха, после охлаждения отфильтровывают от выпавших белковых веществ через бумажный складчатый фильтр и разливают в пробирки по 5 см3, стараясь не смочить горлышка, затем в пробирках пастеризуют.
Предназначается для выращивания дрожжей.
В белое сухое вино добавляют 5–10% сахара. После его растворения среду фильтруют и разливают по пробиркам.
Среда используется для посева дрожжей и уксуснокислых бактерий.
Среда состоит из виноградного сусла – 1/3 объема, сухого вина – 1/3 и водопроводной воды – 1/3 объема. Среду фильтруют и разливают в пробирки.
Рекомендуется для посева уксуснокислых бактерий.
6.1.16. ВИНОГРАДНОЕ СУСЛО РАЗБАВЛЕННОЕ
Сусло разбавляют водой до содержания сахаров 5%, добавляют 1% автолизата дрожжей и доводят рН до 5–6 добавлением 1 Н раствора щелочи.
Среда рекомендуется для молочнокислых бактерий.
В свежий или консервированный яблочный сок добавляют при необходимости сахар до массовой концентрации 10–12 г/100 см3. Концентрация титруемых кислот не должна превышать 6–7 г/дм3. При излишней кислотности сок разбавляют водой.
Стерилизуют в автоклаве текучим паром или в кипятильнике Коха однократно в течение 40–45 мин.
Применяют для культивирования дрожжей.
6.1.18. СМЕСЬ СОЛОДОВОГО СУСЛА С ЯБЛОЧНЫМ
В состав среды входят: солодовое сусло с 5% сухих веществ – 1/2 объема и яблочное сусло – 1/2 объема. Среду осветляют, стерилизуют текучим паром 3 дня подряд по 30 мин.
Предназначается для выращивания молочнокислых бактерий.
200 г измельченной капусты помещают в кастрюлю, заливают 1000 см3 воды и кипятят в течение 10 мин, затем отжимают через двойной слой марли. Полученную жидкость фильтруют и в 2 раза разбавляют водой. К отвару добавляют 2% глюкозы и 1% пептона или 25 см3 солодового сусла (10% СВ) и 1,25 см3 кукурузного экстракта.
Для приготовления среды можно использовать сухую капусту. Измельченную капусту следует сушить в тени при температуре 20–35°С при потоке свежего воздуха. Для приготовления питательной среды 6–8 г сухой капусты кипятят в 1000 см3 воды. Среду разливают в пробирки высоким столбиком по 5–10 см3, стерилизуют в автоклаве при 121°С в течение 30 мин.
Среда предназначена для накопления и выделения молочнокислых бактерий, с добавлением спирта 0,95 см3 на 5 см3 среды.
20 г очищенного от кожуры и протертого сырого картофеля добавляют к 1000 см3 водопроводной воды, настаивают 4 ч, кипятят 15 мин, фильтруют через складчатый фильтр, разливают в пробирки по 5 см3 и стерилизуют при избыточном давлении 0,1 МПа в течение 20 мин.
На 1000 см3 водопроводной воды берут 80 г прессованных дрожжей или 20 г сушеных, смесь кипятят в течение 20 мин, разливают в бутылки и стерилизуют при избыточном давлении 0,1 МПа в течение 30–40 мин.
После отстаивания в течение нескольких дней дрожжевая муть оседает, а дрожжевая вода становится прозрачной.
Вариант 1. Для приготовления можно использовать прессованные или сушеные пекарские дрожжи.
200 г прессованных дрожжей размешивают с 100 см3 водопроводной воды или 100 г сушеных дрожжей с 400 см3 воды, добавляют поваренной соли в количестве 0,15% к весу прессованных дрожжей и 0,5% к весу сушеных дрожжей, смесь помещают в термостат при 50–55°С на 48 ч, затем нагревают до кипения и фильтруют через складчатый бумажный фильтр, разливают в стеклянную посуду и стерилизуют при избыточном давлении 0,1 МПа в течение 30 мин.
Вариант 2. Прессованные дрожжи заливают равным по массе количеством воды: полученную суспензию клеток покрывают тонким слоем толуола и выдерживают трое суток при температуре 60°С, время от времени перемешивая. После этого суспензию несколько минут кипятят, дают остыть и с помощью 1 Н раствора КОН доводят значение рН до 6, затем отстаивают. Надосадочная жидкость (дрожжевой автолизат) должна быть прозрачной, ее сливают и отфильтровывают через бумажный фильтр на воронке Бюхнера под разряжением.
Стерилизуют автоклавированием 20 мин при 112°С.
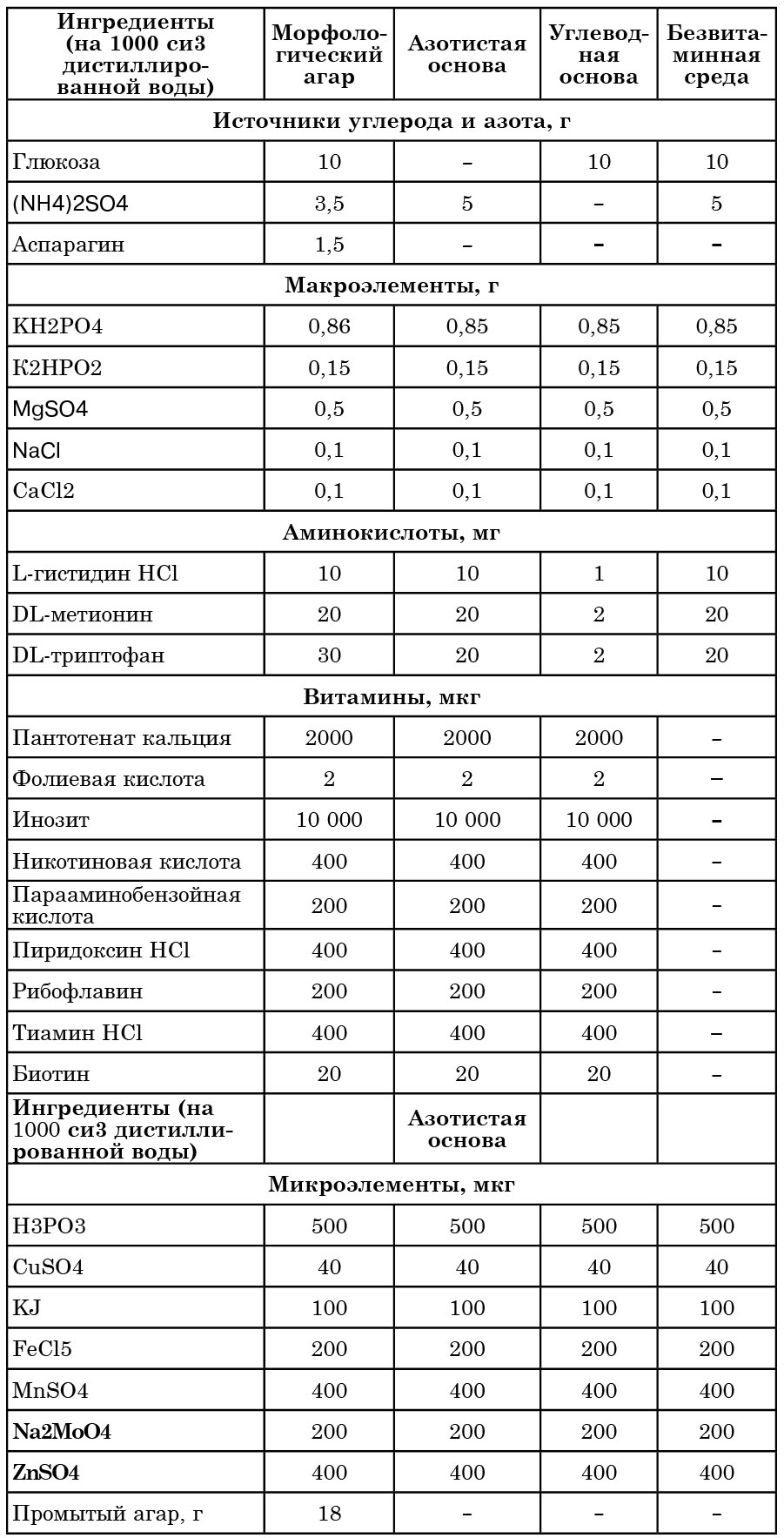
Таблица 6
Состав основных синтетических сред
6.1.23. СТЕРИЛЬНЫЙ МЕЛ
Имеющийся в продаже мелкоразмолотый мел насыпают в стерильные пробирки с ватными пробками по 0,3–0,5 г и стерилизуют сухим жаром 1 ч при 170°С.
6.1.24. СТЕРИЛЬНАЯ ВОДОПРОВОДНАЯ ВОДА
Водопроводную воду разливают в пробирки по 10 или 9 см3 и в колбы по 50 и 100 см3, закрывают ватными пробками и стерилизуют в автоклаве 30 мин при давлении 0,1 МПа или в аппарате Коха при 100°С по 1 ч трое суток подряд.
6.2. СРЕДЫ НАКОПИТЕЛЬНЫЕ ДЛЯ ДРОЖЖЕЙ
Приготовленные среды автоклавируются при 0,1 МПа в течение 20 мин. Могут использоваться как основа для агаризованных сред.
При необходимости вносятся антибиотики.
Состав и количество ингредиентов накопительных сред показаны в таблице 7.
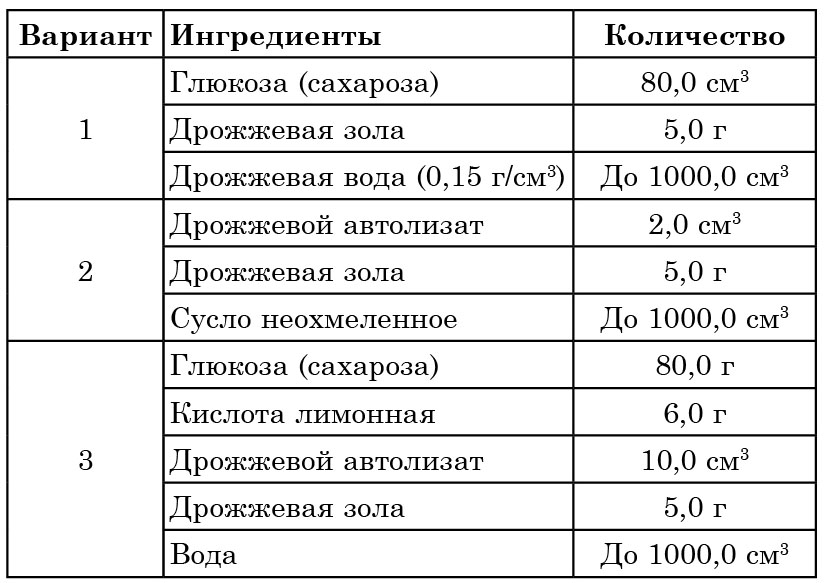
Таблица 7
Среды накопительные для дрожжей
6.3. СРЕДЫ ДЛЯ АСКОСПОРООБРАЗОВАНИЯ
6.3.1. СРЕДА ГОРОДКОВОЙ ДЛЯ ВЫЯВЛЕНИЯ СПОР У ДРОЖЖЕЙ
Состав среды следующий.
Пептон...................................... 1,0 г
Поваренная соль....................... 0,5 г
Глюкоза................................... 0,25 г
Агар .......................................... 2,0 г
Вода............................. до 100,0 см3
Иногда вводят еще 1% мясного экстракта.
Среду нейтрализуют содой (питьевой) до рН 7,3, доводят до кипения и кипятят до тех пор, пока не расплавится агар, фильтруют и разливают в пробирки по 5 см3.
Стерилизуют при избыточном давлении 0,05 МПа в течение 20 мин.
6.3.2. АЦЕТАТНЫЙ АГАР ФОУВЕЛЛА
На 1000 см3 дистиллированной воды берут 5 г CH3COONa·3H2O и 20 г агара. рН среды должно быть 5–7. Автоклавируют 15 мин при 121°С.
6.3.3. АЦЕТАТНЫЙ АГАР МАК-КЛАРИ
CH3COONa·3H2O.......................... 8,2 г
Глюкоза......................................... 1,0 г
KCl................................................. 1,8 г
Дрожжевой экстракт..................... 2,5 г
Агар............................................. 15,0 г
Дистиллированная вода до 1000,0 см3
Автоклавируют 15 мин при 121°С.
6.3.4. СРЕДА С ДРОЖЖЕВЫМ ЭКСТРАКТОМ И ГЛЮКОЗОЙ
Дрожжевой экстракт.................... 5,0 г
Глюкоза....................................... 50,0 г
Агар............................................. 20,0 г
Дистиллированная вода. до 1000,0 см3
Автоклавируют 20 мин при 112°С.
6.3.5. АГАРИЗОВАННАЯ ДРОЖЖЕВАЯ ВОДА
Готовят, добавляя к 1000 см3 дрожжевой воды 15 г агара.
Автоклавируют 15 мин при 121°С.
K2HPO4.............................................................. 1,0 г
CaCl2........................................... 0,05 г
KH2PO4 ....................................... 0,25 г
MgSO4·7H2O............................... 0,25 г
Агар............................................ 20,0 г
Водопроводная вода ..... до 1000,0 см3
Автоклавируют 15 мин при 112°С.
После стерилизации добавляют 6,0 см3 этилового спирта.
Предварительно готовят экстракт овощей путем автоклавирования 10 мин при 112°С равных частей промытых и мелко нарезанных моркови, сахарной свеклы, огурцов и картофеля в четырех частях воды, после чего экстракт отфильтровывают через ткань, отжимая осадок.
К 1000 см3 полученного экстракта (4% СВ, рН 6,7) добавляют 20 г сухих дрожжей и 20 г агара.
Автоклавируют 15 мин при 121°С.
Восемь частей гипса (2CaSO4·H2O) смешивают с тремя частями воды и помещают пасту в цилиндрические формы из бумаги или фольги высотой 3–4 см. Поверхность тщательно сглаживают. После застывания блоки освобождают от форм, помещают в высокие чашки и стерилизуют при 110–120°С в течение 2 ч. Перед посевом в чашки наливают стерильной воды слоем 1 см или раствор, содержащий 1% маннита и 0,5% K2HPO4.
На средах для спорообразования дрожжи инкубируют при температурах, несколько меньших в сравнении с оптимальными для вегетативного роста, – в большинстве случаев при 20–25°С.
Время инкубации составляет до 4–6 недель при еженедельном микроскопировании.
Начинающие исследователи нередко затрудняются отличить аскоспоры от внутриклеточных бесполых спор (эндоспор) или от крупных глобул жира. В таких случаях можно прибегнуть к окраске (см. п. 4.2). Формы спор дрожжей представлены на рисунке 16.
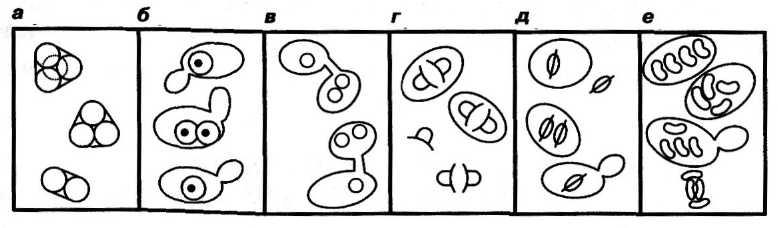
Рис. 16
Споры дрожжей:
а – споры Saccharomyces; б – споры Debaryomyces или Torulaspora; в – споры Zygosaccharomyces; г – шляповидные споры Ptchla membranaefaclens; д – са-турновидные споры Pichía spp. и Williopsis saturnus; е – бобовидные споры Kluyveromyces marxianus и Schizosaccharomyces spp.
Осветленные жидкие, агаризованные или желатиновые среды необходимы в диагностических исследованиях и для получения хорошо видимых признаков глубинного роста и изолированных колоний микроорганизмов.
В ряде случаев прозрачную среду можно получить, отфильтровав ее от осадка через вату. Когда этого бывает недостаточно, среды осветляют с помощью белков куриных яиц. Для осветления 500 см3 среды достаточно белка одного яйца. Белок тщательно отделяют от желтка и встряхивают с равным объемом воды до образования густой пены. Взбитый белок выливают в предварительно расплавленную и затем остуженную до 45–50°С среду. Перед внесением белка проверяют значение рН среды и, если необходимо, среду подщелачивают до рН 7,0–7,3. Среду с белком тщательно перемешивают и прогревают в кипящей водяной бане в течение часа. Белок свертывается и адсорбирует все взвешенные в среде частицы. Среду быстро отфильтровывают в горячем виде через вату.
Синтетические агаризованные среды, внесение белка в которые нежелательно, осветляют следующим образом. Среду, налитую в химический стакан, автоклавируют и оставляют после стерилизации в закрытом автоклаве на 10–12 ч. При таком медленном остывании среды все взвешенные частицы оседают на дно. Застывшую среду извлекают из стакана, прозрачную часть среды срезают, помещают в колбу и вновь стерилизуют.
6.5. ПИТАТЕЛЬНЫЕ СРЕДЫ И УСЛОВИЯ ХРАНЕНИЯ ЧИСТЫХ КУЛЬТУР ДРОЖЖЕЙ
Длительное поддержание чистых культур микроорганизмов, без потери активности и производственных качеств, необходимо как при хранении в коллекциях и проведении научно-исследовательских работ, так и при эксплуатации в производстве.
Основной задачей при хранении чистых культур промышленных штаммов микроорганизмов в музейных коллекциях является правильный выбор условий для сохранения их производственно ценных свойств. Общей тенденцией при этом является максимальное замедление всех жизненных процессов, что достигается различными приемами. Жизнеспособность клеток при этом должна быть сохранена. Кроме того, способы хранения культур должны быть по возможности менее трудоемки и надежны.
Из-за различий биологических свойств видов невозможно использовать с равноценными положительными результатами один общий способ хранения для разных культур дрожжей. Большой опыт по хранению культур микроорганизмов, в том числе и дрожжей, накоплен сотрудниками крупных национальных коллекций, в которых имеется возможность проверять и оценивать разные методы хранения применительно к широкому набору дрожжевых организмов.
Наиболее широко применяемый способ – это поддержание культур путем их периодических пересевов. В последние два десятилетия получили распространение также методы хранения микробных культур под минеральным маслом и лиофильная сушка. Так как эти три метода применяются уже много лет, то имеется возможность сравнительной оценки их пригодности для хранения разных видов дрожжей. Другие, менее широко используемые или недавно разработанные методы можно рекомендовать лишь для проверки с обязательным дублированием культур, которые поддерживаются обычными способами.
Обычно культуры поддерживают, пересевая их на агаризованных средах в двойной повторности. Одна пробирка, которую после засева совсем не открывают, служит контрольной, а из второй по мере надобности делают отсевы.
Частота пересевов. Сроки пересевов определяют для большинства культур дрожжей скоростью высыхания среды. Она зависит от температуры и влажности помещения, где хранят пробирки.
Промежутки между пересевами можно увеличить за счет более плотного закупоривания пробирок и снижения температуры хранения. Так, использование пробирок с завинчивающимися металлическими крышками вместо обычных ватных пробок предохраняет от высушивания, но хуже обеспечивает чистоту сохраняемых культур. Применение вазелинового масла для снижения скорости высыхания культур также имеет свои недостатки, о чем речь будет идти ниже. Поэтому хорошо сделанные ватные пробки (их можно сверху заливать парафином) все же остаются лучшим средством закрывания пробирок. Они обеспечивают достаточный газообмен, хорошо предохраняют от микробного загрязнения и легко изготовляются.
Ватные пробки, однако, не предохраняют культуры от заражения их микофильными клещами (mites). Для профилактики используют следующий прием. Перед посевами или пересевами культур пробку слегка выдвигают из пробирки и наносят на нее каплю раствора, содержащего 10 г сулемы, 50 см3 глицерина, 500 см3 этилового спирта и 450 см3 воды. Затем пробку вдвигают в пробирку и несколько раз проворачивают ее, чтобы смочить внутренние стенки пробирки. В раствор можно добавить какой-либо краситель для контроля равномерности смачивания.
Температура. Если хранение ведется при температуре в пределах 15–20°С, то после пересева пробирки сразу же помещают в коллекционное помещение, за исключением тех культур, которые требуют для роста более высокой температуры. Психрофильные дрожжи выращивают и хранят при 3–4°С в холодильнике. При низкой температуре после появления хорошего роста можно хранить и все другие дрожжи.
Среды. Во многих лабораториях и коллекциях дрожжи поддерживают и хранят на сусло-агаре. Было показано, однако, что на этой сложной среде при длительном хранении происходит изменение физиологических свойств, характерных для вида, за счет адаптации или стабилизации мутантов. В связи с этим для хранения более пригодна среда следующего состава, которую используют для голландской коллекции.
Глюкоза........................................ 4,0 г
Пептон........................................... 0,5 г
Дрожжевая вода
рН 5,8-6,0......................... до 100,0 см3
Для винных дрожжей предложена среда, на которой дрожжи хорошо спорулируют и долго хранятся.
Морковь тертая............................ 125 г
Вода ...................................... 1000 см3
Настоять 1 ч, довести
до кипения, кипятить 10 мин,
отфильтровать через вату, рН 5.
Агар................................................ 30 г
Пивоваренные дрожжи лучше поддерживать на сусло-агаре или среде следующего состава.
Сусло............................................... 3%
Дрожжевой экстракт ....................... 3%
Пептон............................................. 5%
Глюкоза............................................ 1%
Агар ................................................. 2%
На дрожжевых и спиртовых заводах, работающих на мелассе, для хранения производственных культур лучше использовать среду следующего состава.
Мелассовое сусло 5% СВ........ 100 см3
Солодовое сусло 12% СВ........ 100 см3
Дрожжевой автолизат.................. 2 см3
Агар.................................................. 5 г
В некоторых коллекциях дрожжи поддерживают в жидких средах (сусло с дрожжевым автолизатом, пептоном и глюкозой) с пересевами через 4 мес.
6.5.2. ХРАНЕНИЕ ПОД МИНЕРАЛЬНЫМ МАСЛОМ
Заливка агаровых культур минеральным маслом преследует цель задержать высыхание и тем самым увеличить сроки пересевов.
Для заливки культур дрожжей наиболее пригодно высокоочищенное медицинское вазелиновое масло плотностью 0,8–0,9. Масло стерилизуют в автоклаве в течение 1 ч при 121°С, а затем прогревают для удаления влаги в сушильном шкафу при температуре не выше 150°С или выдерживают при комнатной температуре не менее 2–3 дней.
Дрожжи выращивают на сусло-агаре или другой среде, выбранной для хранения.
Среду готовят в пробирках таким образом, чтобы столбик был достаточно высоким, а скос небольшим.
Через 4–6 суток, когда штрих хорошо сформируется, культуры заливают маслом таким образом, чтобы слой его над верхним краем агарового косяка не превышал 1 см. После заливки культуры хранят в вертикальном положении либо при комнатной температуре, либо в холодильнике при 4–6°С.
Пересев дрожжей из-под вазелинового масла производят один раз в год. Для пересевов используют свежие скошенные агаризованные среды, на которых культуры хранились.
Опыт многих коллекций свидетельствует об успешных результатах этого способа хранения дрожжевых культур. Для винных дрожжей, в частности, было показано, что при хранении под вазелиновым маслом с пересевами даже через 2–4 года они не теряют бродильных свойств и хорошо выживают. Имеются указания на сохранение живых клеток дрожжей под маслом до 10 лет и более без пересевов.
К недостаткам этого метода хранения следует отнести следующие:
- при пересевах масло смешивается с инокулятом, и штрихи получаются хуже обычных;
- масло разбрызгивается при обжигании петли, и от этого возникает возможность инфицирования помещения;
- требуется специальная очистка использованных пробирок от масла;
- при стерилизации масла высокими температурами в нем могут образовываться токсичные для дрожжей вещества.
С учетом всех преимуществ при достаточном опыте персонала и правильной организации работы в лаборатории перечисленными недостатками можно пренебречь.***
Лиофилизацией называют процесс высушивания под вакуумом из замороженного состояния. Техника лиофилизации и хранения лиофилизированных культур сильно варьирует в разных лабораториях. Вариации касаются сред и сроков выращивания, применения суспензионных жидкостей, температуры замораживания, условий хранения и восстановления культур.
Дрожжи, подлежащие лиофилизации, выращивают в оптимальных условиях на средах, не слишком обогащенных питательными веществами. Для этой цели пригодна среда Сабуро или глюкозопептонная следующего состава.
Глюкоза........................................................... 1,0 г
Пептон.............................................................. 1,0г
Мясной и дрожжевой
экстракты по.................................................. 0,5 г
NaCl ............................................................... 0,5 г
К2НРO4............................................................. 0,3 г
Агар................................................................. 2,5 г
Вода.................................................... до 100,0 см3
Дрожжи выращивают и на сусло-агаре. Из 2–5-суточных культур готовят густую суспензию в специальных суспензионных жидкостях, содержащих защитные вещества, которые можно разделить на три группы:
- коллоидные среды животного, растительного и минерального происхождения, такие как сыворотка крови, плазма, желатина, снятое молоко, агар-агар, гель гидрата окиси алюминия и др.;
- среды с углеводами (чаще всего 10%-ный раствор сахарозы) и продуктами гидролиза белков – пептоном и аминокислотами;
- сложные среды, в состав которых входят вещества, образующие как коллоидные, так и истинные растворы.
Хорошие результаты получены в голландской коллекции (CBS, г. Дельфт) при использовании в качестве защитной среды раствора, содержащего 7,5% инозита, 2% глутамата натрия и 5% декстрина. рН такой среды доводят до 7,0 с помощью NaOH.
Ниже приведены 2 варианта сложных защитных сред.
Вариант 1.
Желатина......................................................... 1%
Дрожжевой экстракт..................................... 1%
Глюкоза.......................................................... 0,5%
Аскорбиновая кислота............................. 0,25%
Дистиллированная вода................. до 100,0%
рН........................................................................ 5,5
Вариант 2.
Пептон.............................................................. 15 г
Бычья сыворотка..................................... 100 см3
Сахароза.......................................................... 30 г
Дистиллированная вода...................... 200 см3
Использование 10–20%-ного раствора сахарозы дает хорошую выживаемость сразу после лиофилизации, но при длительном хранении жизнеспособность дрожжей резко снижается из-за высокой остаточной влажности материала.
Важным моментом в процессе лиофилизации является замораживание суспензии. Для дрожжей при лиофилизации обычно применяют охлаждение от –30°С до –70°С, однако температура около –15°С, способствующая медленному замораживанию, дает наилучшие результаты. Есть указания также на успешное использование режима быстрого замораживания дрожжей при температуре смеси сухого льда и спирта –78°С и сверхбыстрого замораживания в жидком азоте при –196°С.
Замороженный материал не должен оттаивать в процессе высушивания. Продолжительность высушивания меняют в зависимости от обрабатываемого материала, его объема, состава защитной среды и используемой аппаратуры. Чем мельче кристаллы, образовавшиеся при замораживании, тем быстрее проходит высушивание. Остаточная влажность сказывается на сохранении свойств лиофилизированных дрожжей и на продолжительности последующего их хранения без потери жизнеспособности.
Сразу же после окончания процесса лиофилизации важно определить жизнеспособность обработанной культуры, а в случае, когда была известна концентрация живых клеток в исходной суспензии, можно установить и процентное отношение оставшихся живыми от начального количества клеток.
Реактивацию лиофилизированных культур производят путем переноса части материала либо сразу же в жидкую питательную среду, либо путем предварительного 8-часового выдерживания в дистиллированной воде с последующим пересевом на сусло-агар.
Запаянные ампулы с лиофилизированными культурами хранят в темноте при комнатной температуре или в холодильнике с температурой 4–6°С. Последнее предпочтительнее, особенно для дрожжей с высокой остаточной влажностью материала.
Итоги 19–20-летнего хранения культур дрожжей – представителей 17 родов, всего 557 штаммов – в голландской коллекции позволили установить разную пригодность этого метода хранения для отдельных видов. Дрожжи с мелкими клетками и аскоспорами, такие как Pichia, Hansenula и Debaryomyces, показали хорошую выживаемость, а крупноклеточные слабоспорулирующие или неспорулирующие дрожжи родов Saccharomyces, Kluyveromyces, Dekkera и Brettanomyces выживали хуже.
Таким образом, и этот широко применяющийся сейчас метод хранения микробных культур не следует рассматривать как универсальный, одинаково пригодный для разных видов дрожжей.
6.5.4. МЕТОДЫ КРИОГЕННОГО ХРАНЕНИЯ
Замораживание дрожжей проводят при разных режимах, включая температуры от –10 до –196°С и различные скорости охлаждения. Устойчивость дрожжей к повреждающим эффектам при замораживании повышается при добавлении защитных веществ: глицерина, сахарозы, инозита, диметилсульфоксида, полиэтиленгликоля.
В ампулу объемом 1,2 мл вносят 0,2 мл суспензии клеток дрожжей из стационарной фазы (начальная концентрация клеток 106–108 клеток/см3), 0,5 см3 10%-ного раствора глицерина, 6%-ного инозита или другого защитного вещества. Ампулы запаивают и помещают в жидкостно-фазовый рефрижератор с температурой –70°С со скоростью охлаждения 1–2,5°С в минуту в зоне критических температур — от –5 до –35°С. Замороженные микроорганизмы хранят в жидком азоте при –196°С в металлических контейнерах или стеклянных дьюарах. Существуют контейнеры-рефрижераторы разного объема:
- 10 л на 250 ампул для краткосрочного хранения в экспериментальной работе;
- 35 л на 900 ампул в канистрах;
- 185 л на 12 000 ампул или 1000 штаммов в 12 повторениях.
Для быстрого оттаивания ампулы погружают в водяную баню с температурой 35–45°С на 2 мин. При этом необходимо защитить глаза от возможного взрыва неплотно запаянных ампул. Высев производят на богатую питательную среду.
Трехлетнее хранение пивных дрожжей в жидком азоте показало хорошую их выживаемость без изменения ценных производственных свойств.
6.5.5. ХРАНЕНИЕ НА АДСОРБЕНТАХ
В качестве адсорбентов используют почву, песок, каолин, силикагель, вату и фильтровальную бумагу. Этот способ хранения не имеет разработанной стандартной техники. Высокая выживаемость и физиологическая активность обеспечивается при хранении дрожжей в силикагеле, содержащем различные микроэлементы. Двухсуточные культуры дрожжей, полученные на синтетической среде с 1% парафина на качалках, смешивали со 150 см3 стерильных шариков силикагеля и оставляли в термостате при 32°С на 24 ч. Через сутки определяли рН среды и доводили при необходимости до 7–8. Затем культуральную жидкость сливали, шарики силикагеля с дрожжами помещали в стерильные чашки Петри и высушивали в эксикаторе при пониженном давлении в течение 5–6 суток. После высушивания культуры дрожжей хранили в течение года при комнатной температуре в запаянных стеклянных ампулах при давлении 13,33 кПа. Для реактивации 200 мг шариков силикагеля измельчали в фарфоровой ступке, порошок переносили в
3–5 мл стерильной воды и после кратковременного выдерживания делали высев на питательную среду.
Описан способ хранения дрожжевых культур на вате и полосках фильтровальной бумаги, в 10% -ном растворе сахарозы в почве.
6.5.6. ХРАНЕНИЕ КУЛЬТУР ВИННЫХ ДРОЖЖЕЙ В ВИДЕ СПОР
На сусловых средах винные дрожжи плохо спорулируют и быстро отмирают.
В. В. Абрамовичем был разработан метод получения активно спорулирующих культур для длительного хранения их в состоянии спор.
Дрожжевой осадок из сброженного сусла переносят на 2–3%-ный голодный (водный) агар, где 60–80% клеток образуют споры. Дрожжи сохраняют жизнеспособность на этой среде до двух и более лет. Этим способом было проверено 18 рас винных дрожжей. Подавляющее большинство проверенных культур вызывало активное брожение через
1,5–2,2 года хранения.
Н. И. Бурьян предложила для винных дрожжей способ хранения без потери их основных производственно ценных свойств (энергии размножения и дыхания, бродильной активности, кислотоустойчивости, спиртоустойчивости) путем чередования периодов активного размножения и пребывания в состоянии спор.
Дрожжи предварительно выращивают 48 ч на среде с 5% (по объему) автолизата пивных дрожжей и 2% глюкозы, переносят для спорообразования на измененную среду Адамса (2% агара + 0,14% уксуснокислого натрия), затем 10 суток выдерживают при 15°С, а для длительного хранения переносят в помещение с температурой 10°С. Через 9– 10 мес. дрожжи переводят в активное состояние, засевая споровым материалом колбы со средой, содержащей 18–20% сахара (рН 2,7–3,0), а по окончании брожения – в новую серию колб, среда в которых содержит 28–30% сахара (рН 5,5). Эти пересевы занимают приблизительно 2 мес, после чего дрожжи вновь переносят на голодный агар.
6.5.7. ХРАНЕНИЕ МИКРОБНЫХ КУЛЬТУР ПОД ВАКУУМОМ
(МЕТОД СОРДЕЛЛИ)
Небольшое количество дрожжей с агаровой среды вводят в маленькую пробирку, которую закрывают ватной пробкой. Пробирку помещают в более крупную пробирку из тугоплавкого стекла. На ее дно предварительно вносят несколько стеклянных бус и кристаллов КОН. Пробирку закрывают резиновой пробкой со стеклянной трубкой, через которую производят откачку воздуха до 1,3–6,6 кПа. Трубку запаивают парафином. Пробирки хранят при комнатной температуре.
6.5.8. ХРАНЕНИЕ КОЛЛЕКЦИОННЫХ КУЛЬТУР ДРОЖЖЕЙ В ДИСТИЛЛИРОВАННОЙ ВОДЕ (МЕТОД КАСТЕЛЛАНИ)
Пробирки с 8–10 см3 стерильной дистиллированной воды засевают большим количеством инокулята с глюкозного или суслового агара и хранят при комнатной температуре. По мере испарения воды ее добавляют в пробирки. Жизнеспособность дрожжей сохраняется в этих условиях до двух лет и более. Основным условием успешного хранения дрожжей в дистиллированной воде является обильный инокулят.
Этот способ оказался непригодным для таких слабоспорулирующих дрожжей, как Hanseniaspora, Endomycopsis, Nematospora и некоторых Saccharomyces.
Предлагается способ хранения дрожжей в активной форме, при котором чистую культуру суспендируют в 10%-ном растворе маннита, играющего роль осмотического стабилизатора, с добавлением 0,2% b-фенилэтанола в качестве бактерицидного агента.
При концентрации биомассы дрожжей 1,0–2,5·108 клеток/см3 и температуре хранения 25°С гарантируется сохранение свойств дрожжей в течение года.
6.5.10. ХРАНЕНИЕ МАТОЧНЫХ ХЛЕБОПЕКАРНЫХ И СПИРТОВЫХ ДРОЖЖЕЙ
Маточные дрожжи, обладающие высокой ферментативной активностью, стойкостью и микробиологической чистотой, проявляют хорошую устойчивость при хранении. Но даже незначительные отклонения от требуемых показателей приводят к быстрой потере активности культуры. Для хранения маточных дрожжей ЧК (чистая культура) и ЕЧК (естественно чистая культура) в виде молока устанавливают по два сборника из нержавеющей стали, чтобы создать условия их попеременной мойки и профилактического ремонта. Сборники должны быть снабжены мешалками, охлаждающими системами, указателями уровня и выносными термометрами.
При монтаже сборников предусматривают возможность самостоятельной промывки и пропарки любого участка трубопровода в любом направлении, в том числе и на выпуск в канализацию.
За техническим состоянием коммуникаций, змеевиков и всей запорной арматуры маточного отделения должен быть строгий надзор.
Для стабилизации и улучшения исходных показателей культуры при хранении дрожжей ЧК рекомендуется использовать добавки из расчета на 1 кг прессованных дрожжей (табл. 8).
Таблица 8
Стабилизаторы маточных дрожжей ЧК

На Воронежском дрожжевом заводе смонтирован специальный сборник-термостат, снабженный барботером и охлаждающей рубашкой. К суспензии хранящихся дрожжей добавляют расчетное количество мелассы при температуре 10–12°С, выдерживают 2–3 ч до возникновения слабого спиртового брожения, затем охлаждают до 1°С и хранят при этой температуре. Конвективные токи CO2, выделяющиеся в процессе брожения, удерживают дрожжи во взвешенном состоянии.
Суспензию для засева можно подавать непосредственно из термостата, в котором создается избыточное давление 30 кПа (0,3 кгс/см2), поэтому термостат лучше устанавливать в непосредственной близости к дрожжерастильным аппаратам.
[1] Здесь и далее обозначены методики, разработанные, модифицированные или дополненные автором.










