4.4.1 • Растворение альгината
Чтобы получить раствор альгината, необходимо диспергировать его частицы в данной системе и растворить. Это можно сделать, осторожно добавляя материал в процессе перемешивания с высоким усилием сдвига или предварительно (до внесения в водную систему) смешав альгинат с другими пищевыми ингредиентами. Обычно сухой порошок альгината смешивают с частицами сахара или суспендируют в гидрофобном растворителе (например, растительном масле). Скорость растворения альгината зависит от размера его частиц - чем они меньше, тем быстрее осуществляется растворение (рис. 4.4). Вместе с тем мелкие частицы альгината склонны к агломерации и комкованию, из-за чего необходимо тщательно их диспергировать и перемешивать [27]. На скорость растворения альгината влияют содержание СВ, концентрация ионов в воде (ее жесткость) и температура.
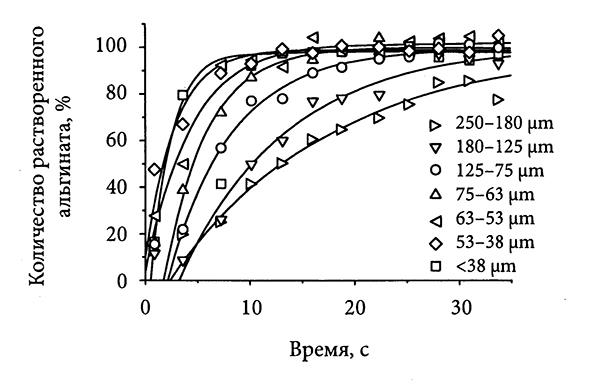
Рис. 4.4. Растворение поршкового альгината с частицами разных размеров
4.4.2. Вязкость
Вязкость раствора альгината определяется длиной молекулы этого полимера, причем наблюдается четкая корреляция вязкости раствора альгината в чистой воде и молекулярной массы по уравнению Марка-Хоувинка-Сакурады (MHS). Способы определения вязкости растворов альгинатов и ее значения для растворов продуктов из Laminaria hyperborea (стебель) и Macrocystispyrifera описаны в работе [29]. Молекулярно-массовое распределение можно определить методом эксклюзионной хроматографии (SEC-MALLS) [49].
Вязкость, определяемая с помощью реометра или вискозиметра, зависит также от состава водной системы, на который влияют присутствие солей, Сахаров, а также одно- и многоатомных спиртов. Введение малых количеств солей кальция приводит к резкому увеличению вязкости раствора благодаря частичной и непостоянной сшивке макромолекул.
Вязкий раствор альгината обладает свойством разжижаться при сдвиге. Это свойство определяется наличием длинных полимерных цепей и жесткостью гидратированных молекул. Альгинат - это линейный полисахарид с большим зарядом, что придает молекулам жесткость. При низких скоростях сдвига (например, при хранении или перемешивании на малой скорости) молекулы ориентированы более или менее случайно, но при увеличении скорости сдвига молекулы начинают ориентироваться параллельно одна другой. Следовательно, когда скорость сдвига выйдет за границы начальной ньютоновской области, кажущаяся вязкость будет уменьшаться. Эффект разжижения при сдвиге зависит от концентрации солей в растворе, поскольку ионы экранируют заряд молекулы альгината и уменьшают жесткость молекулы.
Низкомолекулярные альгинаты хранятся дольше, так как на их кажущуюся вязкость распад цепей влияет меньше, чем у высокомолекулярных.
Требуемую вязкость можно получить, зная свойства различных промышлен- но выпускаемых альгинатов. Высоко- и низкомолекулярные сорта дают разную текстуру, так что варьируя концентрации альгината, можно регулировать текстурные и реологические свойства. Зависимость вязкости растворов альгинатов от концентрации и молекулярной массы приведена на рис. 4.5. Чтобы снизить вязкость продукта, можно использовать больше альгината с низкой вязкостью или меньше высоковязкого.
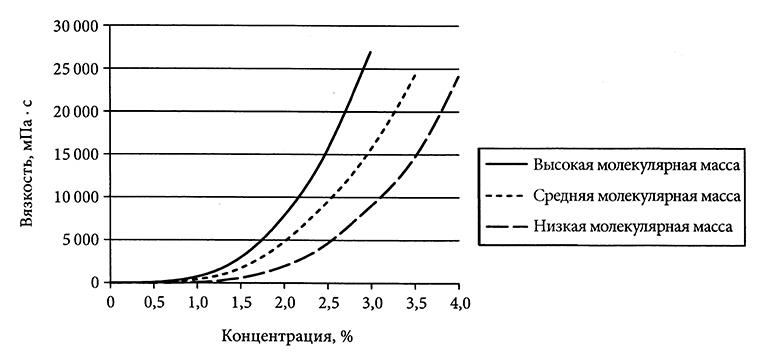
Рис. 4.5. Зависимость вязкости альгинатов от концентрации и молекулярной массы.
Низкомолекулярные альrинаты хранятся дольше, так как на их кажущуюся вязкость распад цепей влияет меньше, чем у высокомолекулярных.
4.4.3. Гелеобразующие свойства
Наиболее важным свойством альгинатов, обусловленным их блочной структурой, является способность к гелеобразованию. Главное преимущество альгината как гелеобразователя состоит в том, что он дает термостойкие гели, затвердевающие при комнатной температуре. В пищевой промышленности используется в основном гелеобразование в присутствии ионов кальция, однако в слабокислой среде (например, во фруктовых продуктах и джемах) альгинат образует гели кислотного или смешанного кальциево-кислотного типа (об этом см. далее).
Чтобы прореагировать с ионами кальция и сформировать гель, в блоках альгината должно быть определенное количество остатков гулуроновой кислоты. В гелевой сетке альгината узловая зона образуется в месте физического соединения G-блока одной молекулы альгината с С-блоком другой молекулы путем взаимодействия «цепь-Са2+-цепь». М- и МG-блоки не входят в узловые зоны, но образуют в гелевой сетке так называемые «эластичные» сегменты.
Взаимодействие альгината с ионами кальция можно представить на примере модели «яичного лотка», в которой ионы кальция, как яйца в лотке, занимают пустоты в альгинатной цепи [18] (рис. 4.6). Адекватность указанной модели доказана на основании данных о потенциалах Леннард-Джонса, силах Ван-дер-Ваальса и электростатических взаимодействиях [2]. Наиболее вероятной структурой в геле является ассоциат из двух гулуронатных блоков с антипараллельными цепями, причем форма этой структуры аналогична строению яичного лотка. Позднее методом малоуглового рентгеновского рассеяния было показано [41], что при увеличении концентрации ионов кальция и/или содержания С-блоков в альгинате толщина узловых зон возрастает.
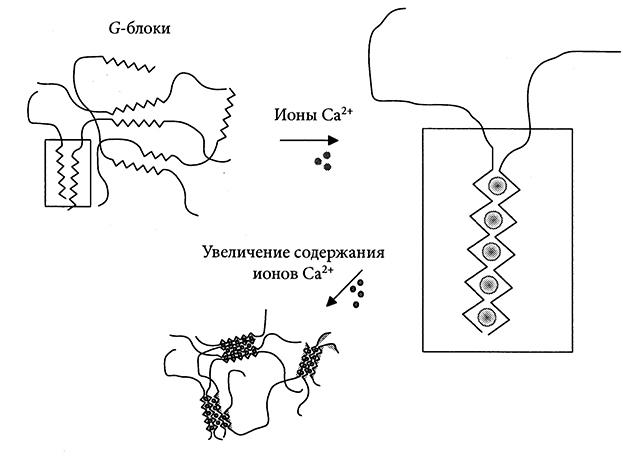
Рис. 4.6. Образование альгинатного геля в присутствии ионов кальция
(модель «яичного лотка»).
Эта зависимость объясняется тем, что в латеральных узловых зонах соединяется более двух С-блоков, то есть эти зоны становятся многослойными и, следовательно, в данном случае исходную модель «яичного лотка» необходимо модифицировать.
Способность к гелеобразованию и прочность альгинатного геля во многом зависят от числа и длины узловых зон, то есть от количества и средней длины G-блоков. Наиболее высокой реакционной способностью по отношению к ионам кальция и самой сильной способностью к гелеобразованию обладают альгинаты с высоким содержанием длинных G-блоков. На гелеобразование влияют также молекулярная масса альгината и количество ионов кальция. В низкомолекулярных альгинатах (молекулярной массой до 100-150 кДа) прочность насыщенных кальцием гелей существенно возрастает по мере увеличения молекулярной массы полимера, однако при молекулярной массе более 100-150 кДа прочность геля при увеличении молекулярной массы возрастает незначительно [11, 39].
С химической точки зрения образование кальциево-альгинатного геля следует рассматривать как ионообменный процесс: противоион водорастворимого альгината обменивается на кальций, то есть происходит перенос «золь-гель». Противоион (например, натрия) имеет более низкое сродство к альгинату, чем ион кальция. Сродство натрия к альгинату, однако, выше, чем у калия [12], что может иметь практическое значение, в частности, для приготовления гелей с малым содержанием кальция (здесь следует отметить, что при высоком содержании кальция влияние противоио- нов невелико). Благодаря различиям в сродстве ионов натрия и калия кальциевый альгинат образуется из калиевого немного быстрее, чем из натриевого. Использование альгината калия может оказаться более предпочтительным в системах с высоким количеством ионов натрия (например, когда полученные гели хранятся в рассолах), поскольку обратный обмен натрия на кальций снижается и минимизируется последующее снижение прочности геля.
Кислотный альгинатный гель также образуется при участии узловых зон. Гелеобразование и прочность геля зависят прежде всего от G-блоков [10, 13]. М-блоки также участвуют в гелеобразовании, формируя слабые сшивки между цепями, а чередующиеся МG-блоки образованию межмолекулярных сшивок препятствуют.
4.4.4. Синерезис
Несмотря на то что после гелеобразования молекулы воды удерживаются сеткой альгинатного геля, у них сохраняется способность к диффузии. Гель сохраняет воду, образуя с ней водородные связи, но если гелевая сетка сжимается, то часть воды из нее вытесняется. Этот эффект, называемый синерезисом, наблюдается во многих биополимерных гелевых системах. В альгинатных гелях синерезис зависит от соотношения М : G, от концентрации ионов кальция, механизма затвердевания и молекулярной массы. Для устранения нежелательного синерезиса все эти факторы необходимо контролировать.
Гели из низкомолекулярных альгинатов менее склонны к синерезису, чем более высокомолекулярные (по-видимому, из-за меньшего числа неповрежденных эластичных сегментов между узловыми зонами, что делает гель менее способным к реорганизации и сжатию в ходе продолжающегося процесса гелеобразования). В большей степени подвержены синерезису альгинаты с большим количеством чередующихся МG-структур и с более гибкими эластичными сегментами в гелевой сетке [9]. Наиболее важным фактором является соотношение содержания ионов кальция и альгината. При соблюдении баланса, то есть при содержании ионов Са2+, достаточном для насыщения всех G-блоков, синерезис практически не проявляется. При избытке же ионов кальция синерезис становится заметнее. «Внутреннее» гелеобразование обычно дает гели, менее склонные к синерезису, чем при «внешнем» гелеобразовании. Это объясняется в основном тем, что соотношение концентраций ионов кальция и альгината можно контролировать относительно легко.
4.4.5. Измерение прочности геля
Важной характеристикой гелей, приготовленных из альгинатов различного происхождения и имеющих разное соотношение М: С, является прочность геля. Промышленного стандарта для измерения прочности геля не существует, и обычно прочность геля измеряют по силе, необходимой для поворота зонда в 0,7-1,0%-ных альгинатных гелях или для сжатия геля. Значения прочности геля, рекомендуемые Научно-исследовательской ассоциацией пищевой промышленности (FIRA, Food Industries Research Association) получены для гомогенных альгинатных гелей внутреннего затвердения с использованием тестера, разработанного этой организацией [44]. Сила, требуемая для сжатия геля, может быть измерена также приборами Instron или анализатором текстуры (Texture Analyzer).







