4.1. ПРОСТАЯ ОКРАСКА МИКРООРГАНИЗМОВ
Мазок, т. е. каплю эмульсии микроорганизмов, помещенную на предметное стекло, высушивают и фиксируют над пламенем горелки. Подготовленный препарат заливают 1–2 каплями краски (метиленовой синью Леффлера или фуксином Пфейфера), выдерживают 0,5–1 мин и смывают дистиллированной водой.
Фиксированный на пламени препарат заливают 5%-ным водным раствором малахитового зеленого и 3–4 раза прогревают до появления паров (30–60 с). Окраску можно проводить, выдерживая препарат 3–5 мин в растворе малахитового зеленого, подогретого до 80°С. Затем препарат промывают 30 с в проточной воде и докрашивают 30 с 0,5%-ным водным раствором сафранина.
Зрелые аскоспоры окрашиваются в сине-зеленый, а вегетативные клетки – в красный цвета.
Аскоспоры дрожжей родов Hansenula, Schizosaccharomyces могут удерживать оба красителя.
4.2.2. КАРБОЛ-ФУКСИНОВАЯ ОКРАСКА
Вариант 1. Фиксированный на пламени препарат заливают раствором Циля (10 см3 насыщенного спиртового раствора основного фуксина с 90 см3 5%-ного фенола) и нагревают 2–5 мин до появления паров. Затем проводят обесцвечивание препарата, погружая его в 2%-ный раствор молочной кислоты или в 95%-ный этанол, содержащий 1 мл концентрированной НСl в 100 см3.
Препарат промывают в воде и докрашивают 3–5 мин 1%-ными растворами метиленового синего или нильского голубого.
Зрелые аскоспоры окрашиваются в красный, вегетативные клетки – в синий цвета.
Аскоспоры рода Schizosaccharomyces, а также после набухания аскоспоры дрожжей родов Hansenula и Pichia не обладают кислотоустойчивостью и окрашиваются в синий цвет.
Вариант 2. Фиксированный препарат окрашивают в течение 2–3 мин карболовым фуксином при подогревании над пламенем горелки, затем краску сливают и препарат обесцвечивают соляной кислотой со спиртом (две части 10%-ного раствора соляной кислоты и одна часть 96%-ного спирта) в течение 30 с, промывают водой и окрашивают в течение 1–2 мин метиленовой синью.
Споры окрашиваются в красный цвет, а вегетативные клетки – в синий.
4.3. ОПРЕДЕЛЕНИЕ ГЛИКОГЕНА В КЛЕТКАХ ДРОЖЖЕЙ
Гликоген – одно из резервных веществ дрожжевых клеток. Он накапливается в цитоплазме и окрашивается раствором Люголя в коричневый или красно-бурый цвет. Наблюдения за содержанием гликогена в клетках дрожжей проводят в динамике развития культуры.
Таблица 4
Содержание гликогена в клетках
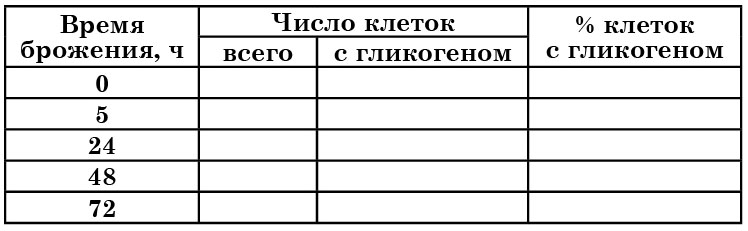
Готовят препарат «раздавленная капля» в растворе Люголя и в нескольких полях зрения подсчитывают общее количество клеток и количество клеток, содержащих гликоген. Общее число подсчитанных клеток должно быть не менее 100.
Полученные данные можно регистрировать в предлагаемой таблице 4.
Если препарат нагреть до 60°С, окраска гликогена исчезает, а при охлаждении препарата она вновь восстанавливается.
На предметном стекле готовят тонкий мазок из культуры исследуемых дрожжей, высушивают на воздухе и фиксируют на пламени горелки. Мазок окрашивают карболовым фуксином 30–40 с и промывают водой. Далее мазок дифференцируют, погружая его в склянку с 1%-ным раствором серной кислоты на 20–30 с и немедленно промывают водой. Серная кислота обесцвечивает цитоплазму, а зерна волютина остаются окрашенными фуксином. Препарат докрашивают метиленовым синим (1:40) 20–30 с, промывают водой, высушивают на воздухе и микроскопируют, пользуясь объективом МИ-90.
На препарате зерна волютина окрашены в красный цвет, цитоплазма клетки – в голубой.
Тонкий фиксированный мазок культуры исследуемых дрожжей окрашивают метиленовым синим Леффлера в течение 3 мин. Мазок промывают водой, не высушивая, покрывают его покровным стеклом и микроскопируют, пользуясь объективом ВИ-60.
На препарате зерна волютина окрашены в красновато-фиолетовый цвет, цитоплазма – в голубой.
Для более ясной дифференциации зерен волютина под покровное стекло полоской фильтровальной бумаги протягивают каплю 1%-ного раствора серной кислоты. При этом зерна волютина сохраняют окраску, а цитоплазма обесцвечивается.
Обратный результат можно получить, добавляя под покровное стекло каплю 5%-ного раствора соды. Волютиновые зерна обесцвечиваются, а цитоплазма клетки сохраняет голубой цвет.
4.5. ОКРАСКА МИКРООРГАНИЗМОВ ПО ГРАМУ
Препарат, фиксированный в пламени горелки или обработанный метиловым спиртом, покрывают раствором генцианвиолета на 1–2 мин, затем обрабатывают в течение 1–2 мин раствором Люголя, промывают водой и быстро опускают в 96%-ный этиловый спирт. В спирте препарат держат до тех пор, пока от него не перестанет отходить краска. После этого препарат вновь промывают водой и окрашивают разбавленным фуксином Пфейфера в течение 0,5–1 мин.
Грамположительные бактерии окрашиваются в темно-фиолетовый цвет, грамотрицательные – в красный.
Метод применяется исключительно для окраски бактерий и не эффективен при окрашивании дрожжей, ввиду принципиальных отличий в строении клеточной стенки.
Метиленовый синий (насыщенный спиртовой раствор). К 100 см3 96%-ного этилового спирта прибавляют 10 г метиленового синего (в порошке) и оставляют стоять несколько дней (при этом несколько раз встряхивают), затем раствор фильтруют.
Метиленовый синий 1:40.
Метиленовый синий
(насыщенный спиртовый раствор) 1 см3
Вода дистиллированная............... 40 см3
Метиленовый синий щелочной (синька Леффлера). В 100 см3 дистиллированной воды растворяют 30 см3 насыщенного спиртового раствора метиленового синего и 1 см3
1%-ного раствора едкого кали.
Разбавленная синька (по Финку). Готовят три раствора: 0,09 г фосфорнокислого натрия (N2HPO4) растворяют в 500 см3 дистиллированной воды; 13,6 г фосфорнокислого калия (KH2PO4) растворяют в 500 см3 дистиллированной воды; 0,1 г метиленового синего растворяют в 500 см3 дистиллированной воды.
Для приготовления рабочего раствора синьки смешивают 0,25 см3 первого раствора с 99,75 см3 второго и 100 см3 раствора синьки, рН раствора должно быть 4,6.
Основной фуксин. 2 г сухой краски и 20 см3 96%-ного этилового спирта встряхивают и оставляют стоять несколько дней, получается насыщенный спиртовой раствор.
Карболовый фуксин (по Цилю). 10 см3 насыщенного спиртового раствора основного фуксина растворяют в 100 см3 5%-ного раствора карболовой кислоты (фенола).
Разбавленный фуксин (по Пфейферу). Для окраски микроорганизмов применяют раствор разбавленного в 10 раз карболового фуксина.
Малахитовый зеленый (водный насыщенный раствор).
Малахитовый зеленый................ 5 г
Дистиллированная вода...... 100 см3
Для окраски спор лучше брать спиртово-водный раствор.
Малахитовый зеленый................ 5 г
Спирт этиловый, 96°............. 20 см3
Дистиллированная вода........ 80 см3
Сафранин (водный раствор).
2,5%-ный раствор сафранина
в 96%-ном этаноле ............... 10 см3
Вода дистиллированная...... 100 см3
Насыщенный спиртовой раствор генцианвиолета (для окраски по Граму).
1 г сухой краски растворяют в 10 см3 96%-ного спирта и смешивают со 100 см3
5%-ного раствора карболовой кислоты; для достижения прозрачности добавляют несколько капель спирта.
Растворы йода в йодистом калии (по Люголю).
Раствор Люголя для окраски по Граму. Для приготовления раствора Люголя 1 г кристаллического йода растирают в фарфоровой ступке с 2 г йодида калия и порциями (по 5 см3) добавляют дистиллированную воду до полного растворения кристаллического йода в йодиде калия. После полного растворения кристаллов объем доводят до 300 см3. Приготовленный раствор Люголя хранят в посуде из темного стекла (на свету раствор Люголя быстро обесцвечивается).
Раствор Люголя для выявления гранулезы.
Кристаллический йод.................. 1 г
Йодид калия ................................ 2 г
Дистиллированная вода...... 100 см3
Гранулеза в клетках окрашивается в темно-синий цвет.
Раствор Люголя для выявления гликогена.
Кристаллический йод.................. 7 г
Йодид калия .............................. 20 г
Дистиллированная вода...... 100 см3
Гликоген приобретает красно-бурую окраску.
Техника приготовления растворов для выявления гранулезы и гликогена такая же, как раствора Люголя для окраски по Граму.
Раствор туши.
Традиционный метод.
Жидкая натуральная тушь.... 10 см3
Дистиллированная вода........ 90 см3
Раствор центрифугируют 15–20 мин. Верхний слой отсасывают (пипеткой), переносят в пробирку и автоклавируют 30 мин при 0,05 МПа (температура 110°С).
Можно раствор туши сразу после смешивания автоклавировать 30 мин при давлении 0,05 МПа. После автоклавирования раствор отстаивают две недели, после чего его можно использовать.
Метод Литтмана.
Черная тушь.......................... 15 см3
Раствор тимерсола
в соотношении 1:1000........... 30 см3
Твин-80.................................. 0,1см3
На черном фоне капсулы видны как светлый ореол вокруг клетки.







