Методики определения редуцирующей способности
и глюкозного эквивалента (ГЭ) в продуктах гидролиза крахмала
По методу Лэйна-Эйнона [ 176]
1. Область применения
Метод применим для всех продуктов гидролиза крахмала.
2. Принцип
Метод постоянного титра Лэйна-Эйнона. Метод основан на титровании смеси реактива Фелинга (Фелинговой жидкости) с исследуемым образцом в присутствии индикатора метиленового голубого.
3. Реактивы
3.1. Раствор А. Растворить в дистиллированной воде 69,3 г сульфата меди (II) пентагидрата (CuS04 * 5Н20), довести объем раствора дистиллированной водой до 1000 см3.
3.2. Раствор Б. Растворить в дистиллированной воде 346 г тартрата калия натрия тетрагидрата (KNaC4H406 • 4Н20) и 100,0 г гидроксида натрия (NaOH), довести объем раствора дистиллированной водой до 1000,0 см3. Перед использованием декантировать раствор с осадка (при необходимости).
3.3. Индикатор метиленовый голубой (C16H18CIN3S • 2Н20), 1%-й водный раствор.
3.4. Безводная D-глюкоза для анализа. Перед использованием сушить два часа при 100 °С и охладить в эксикаторе.
3.5. Стандартный раствор глюкозы. Взвесить с точностью до 0,1 мг 1,25 г высушенной по п. 3.4 безводной D-глюкозы и растворить в дистиллированной воде, довести объем раствора дистиллированной водой до 250 см3.
4. Аппаратура
4.1. Автоматическая бюретка.
4.3. Бюретка на 50 см3 с ценой деления 0,1 см3.
4.3. Горелка Бунзена.
4.4. Эксикатор с осушителем.
4.5. Аналитические весы с ценой деления 0,1 мг.
5. Выполнение анализа
Приготовить и нормализовать реактив Фелинга. Реактив Фелинга не подлежит хранению.
А. Нормализация
Приготовить реактив Фелинга: в коническую колбу объемом 250 см3 налить 12,5 см3 раствора А, затем 12,5 см3 раствора Б и хорошо перемешать.
Наполнить бюретку на 50 см3 стандартным раствором глюкозы. Прилить к реактиву Фелинга 23,5 см3 стандартного раствора глюкозы из бюретки. Добавить несколько стеклянных шариков для равномерного кипения и поставить колбу на проволочную сетку, накрытую чистым асбестом. Нагреть на горелке Бунзена. Кипятить две минуты и добавить три капли метиленового голубого.
Добавить, не прерывая кипения, две-три капли раствора глюкозы с интервалами примерно 10 с до полного исчезновения синего окрашивания. Отметить изменение окраски в чистой жидкости над осадком от светло-синей до бесцветной.
Необходимо пользоваться непрямым искусственным освещением. Рассеянный дневной свет непригоден для определения конечной точки титрования.
Титрование должно быть закончено в течение минуты. Повторить титрование дважды.
Для титрования должно быть использовано ровно 24,1 см3 стандартного раствора глюкозы - в противном случае необходимо соответствующим образом отрегулировать концентрацию раствора А (п. 3.1) и повторить нормализацию.
В. Измерение
Тщательно отвесить в мерный стакан навеску образца. Примерную массу навески т рассчитывают таким образом, чтобы раствор содержал приблизительно 1,25 г редуцирующих Сахаров:
m = 12 500 / предп. ГЭ • СВ.
Растворить образец в дистиллированной воде и довести объем раствора дистиллированной водой до 250 см3. Повторить операции п. А, используя для титрования вместо стандартного раствора глюкозы раствор образца. Зарегистрировать количество раствора образца, израсходованного на титрование, см3.
6. Обработка результатов
Глюкозный эквивалент (ГЭ) вычисляют по формуле
![]()
где а - глюкозный фактор из нижеследующей таблицы (табл. П 3.1, 2-й столбец), определяемый по объему раствора, израсходованного на титрование (см. табл. П 3.1, 1-й столбец); V - объем раствора образца, израсходованного на титрование, см3; т - масса образца, растворенного в 250 см3 воды, г; СВ - содержание сухих веществ в образце, % .
За результат испытаний принимается среднее арифметическое двух параллельных измерений. Вычисление проводят с точностью до первого десятичного знака.
7. Примечание
Альтернативный метод: вычисление ГЭ по пикам Сахаров на хроматограмме, полученной методом гель-проникающей хроматографии (ГПХ).
8. Ссылка
Международный стандарт ISO 5377.
Lane, J.H., Eynon, L. (1923). Determination of reducing sugars by means of Fehling's solution with methylene blue as internal indicator / J. Soc. Chem. Ind. Trans. P. 32-36.
- Таблица П 3.1
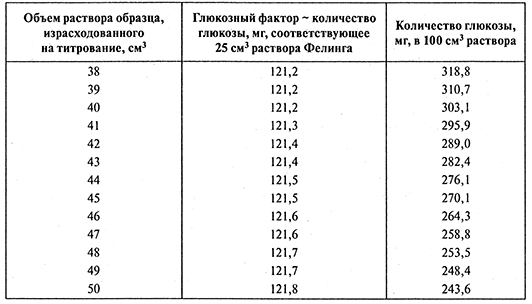
Примечание. Все значения относятся к безводной глюкозе.
По методу Луффа-Скурла [176]
1.Область применения
Метод применим для всех продуктов гидролиза крахмала.
2.Принцип
Метод основан на йодном титровании избытка меди
3.Реактивы
3.1. Раствор Луффа:
3.1 а. Растворяют 50 г лимонной кислоты (С6Н807 • Н20), ч. д. а., в 50 см3 дистиллированной воды.
3.1б. Растворяют 143,7 г карбоната натрия (Na2C03), ч. д. а., в 400-500 см3 кипящей дистиллированной воды.
После охлаждения раствора карбоната натрия осторожно смешивают растворы 3.1 а и 3.16.
3.1с. Растворяют 25 г сульфата меди (CuS04 • 5Н20), ч. д. а., приблизительно в 100 см3 дистиллированной воды и вливают в смесь растворов 3. la и 3.16. Доводят объем раствора до 1 дм3 дистиллированной водой.
3.2. Уксусная кислота - 0,4 н раствор: 24 см3 уксусной кислоты (СН3СООН), ч. д. а., разводят дистиллированной водой до 1 дм3.
3.3. Йод - 0,1 н раствор (стандартный раствор для титрования).
3.4. Соляная кислота - 0,75 н раствор: 73 г концентрированной соляной кислоты (НС1) разводят дистиллированной водой до 1 дм3.
3.5. Тиосульфат натрия - 0,1 н (стандартный раствор для титрования).
3.6. Раствор крахмала: 2 г растворимого крахмала растворяют в 100 см3 дистиллированной воды. Консервируют небольшим количеством HgO.
3.7. Раствор образца: предварительно оценивается ГЭ образца и вычисляется количество, необходимое для расходования приблизительно 15 см3 раствора тиосульфата натрия. Отвешивают образец в мерную колбу на 250 см3. Растворяют в дистиллированной воде и доводят дистиллированной водой до метки.
4.Аппаратура
4.1. Электрическая плитка.
5.Выполнение анализа
Перенести с помощью пипетки 25 см3 раствора Луффа и 25 см3 раствора образца в коническую колбу на 300 см3. Опустить в колбу стеклянные шарики. Нагревать на электрической плитке в течение ~3 мин до кипения. Кипятить с обратным холодильником ровно 10 мин (использовать таймер). Промыть холодильник небольшим количеством дистиллированной воды. Быстро охладить раствор холодной водой.
Добавить 50 см3 уксусной кислоты из мерного цилиндра. Прилить с помощью пипетки 25 см3 0,1 н раствора йода. Добавить мерным цилиндром 55 см3 0,75 н раствора НС1. Встряхивать до полного растворения. Титровать тиосульфатом натрия с 6-8 каплями раствора крахмала в качестве индикатора до появления медно-синей окраски.
Провести холостой опыт с 25 см3 дистиллированной воды вместо раствора образца.
6.Обработка результатов
Глюкозный эквивалент (ГЭ) в пересчете на сухое вещество вычисляют по формуле
![]()
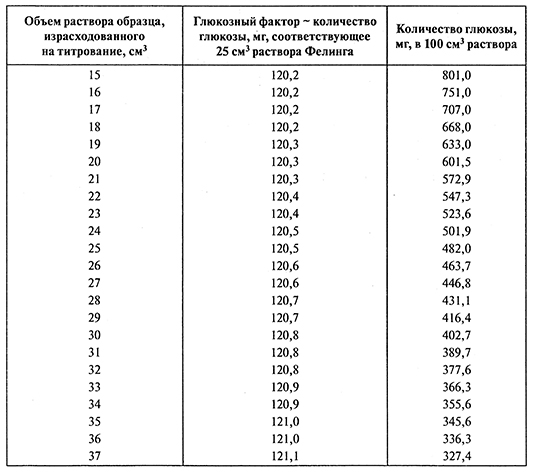
где с - количество глюкозы на 25 см3 раствора образца, мг, определяемое поданным табл. П 3.2, с использованием титра Т; т - масса образца, г; СВ - содержание сухого вещества в образце, %;
![]()
Здесь Vo - объем 0,1 н раствора тиосульфата натрия, израсходованного в холостом опыте, см3; V- объем 0,1 н раствора тиосульфата натрия, израсходованного на титрование образца, см3; К - поправочный коэффициент раствора тиосульфата натрия.
За результат испытаний принимается среднее арифметическое двух параллельных измерений. Вычисление проводят с точностью до первого десятичного знака.
7.Примечание
Альтернативный метод: вычисление ГЭ по пикам Сахаров на хроматограмме, полученной методом ГПХ.
8.Ссылка
Международный стандарт ISO 5377.
Schoorl N. (1929). Suiker titratie / Chemisch Weekblad, 130-134 and ZLUF 57,566 (1929).
- Таблица П 3.2