НИТРАТЫ И НИТРИТЫ
Широко распространены в окружающей среде, главным образом в почве и воде. Наряду с нитратами в почве содержится другой минеральный источник азота – аммоний. Последний адсорбируется почвой и нитрифицируется. Ион NO3 почвой не поглощается, поэтому весь нитратный азот находится в почве в растворе, легко подвижен и доступен для растений. Нитраты быстро и легко реагируют с другими компонентами почвы.
Растения ассимилируют нитраты с помощью корневой системы двумя путями:
- восстановлением нитратов в нитриты с помощью нитрат-редуктазы НАДФ Н;
- восстановлением нитратов в аммиак с помощью нитрит-редуктазы.
Нитритов в растениях содержится небольшое количество, в среднем 0,2 мг/кг, поскольку они представляют собой промежуточную форму восстановления окисленных форм азота в аммиак.
Концентрация нитратов в растениях колеблется от нескольких до тысяч миллиграммов, зависит от многих факторов, среди которых определяющим является увеличение нитратов в почве за счет интенсификации процесса нитрификации или – особенно – в связи с неконтролируемым использованием азотных удобрений.
Отмечено, что некоторые пестициды, другие токсические соединения, нарушая обмен веществ в растениях, усиливают накопление нитратов, например гербицида 2,4-Д – в 10-20 раз.
В табл. 35 и 36 представлены данные Института питания РАМН о содержании нитратов и нитритов в пищевых продуктах. Из таблиц видно, что наибольшие концентрации нитратов встречаются в зелени, овощах, особенно корнеплодах, бахчевых культурах.
Необходимо отметить, что парниковая зелень отличается более высоким содержанием нитратов, что объясняется интенсивным удобрением почвы и недостаточным освещением. Содержание нитритов в пищевых продуктах может возрастать по мере их хранения. Это связано с развитием микрофлоры, способной восстанавливать нитраты. Восстанавливающими свойствами обладают многие представители лактобацилл, E. coli, Ps. fluorescens, некоторые виды стрептококков, B. subtilis, другие микроорганизмы. В этой связи детям рекомендуется употреблять сок в течение 1 ч после его приготовления.
Кулинарная обработка пищевых продуктов снижает содержание в них нитратов: очистка, мытье и вымачивание – на 5-15 %, варка – до 80 % (в связи с переходом нитритов в отвар, инактивацией ферментов, восстанавливающих нитраты в нитриты). При более жесткой тепловой обработке нитраты разрушаются с образованием оксидов азота и кислорода.
Механизм токсического действия нитритов на организм заключается в их взаимодействии с гемоглобином крови. В результате окисления двухвалентного железа до Fe (III) образуется метгемоглобин, который в отличие от гемоглобина не способен связывать и переносить кислород. Развивается клиническая картина гипоксии. 1 мг нитрита натрия может перевести в метгемоглобин около 2000 мг гемоглобина.
ДСД нитрита – 0,2 мг/кг массы тела, за исключением детей грудного возраста. Острое отравление отмечается при одноразовой дозе 200-300 мг, летальный исход – 300-2500 мг. Токсичность нитритов зависит от состава рациона, индивидуальных особенностей организма, в частности, от активности метгемоглобинредуктазы, обладающей способностью восстанавливать метгемоглобин в гемоглобин.
Наряду с клиническими проявлениями интоксикации (обильное потение, синюшность кожи, одышка, головокружение) хроническое воздействие нитритов приводит к снижению содержания в организме витаминов A, E, C, B1, B6. С этим связывают снижение устойчивости организма к воздействию различных факторов, в том числе онкогенных.
Нитраты, в отличие от нитритов, не являются метгемоглобинообразователями и не обладают выраженной токсичностью. Острые отравления наблюдаются у людей при случайном приеме 1–4 г нитратов, доза 8–14 г может оказаться смертельной. Главной причиной острой интоксикации является восстановление нитратов в нитриты, что может происходить в пищевых продуктах или пищеварительном канале.
Таблица 35
Содержание нитратов в продовольственном сырье и пищевых продуктах (в пересчете на нитрат-ион)
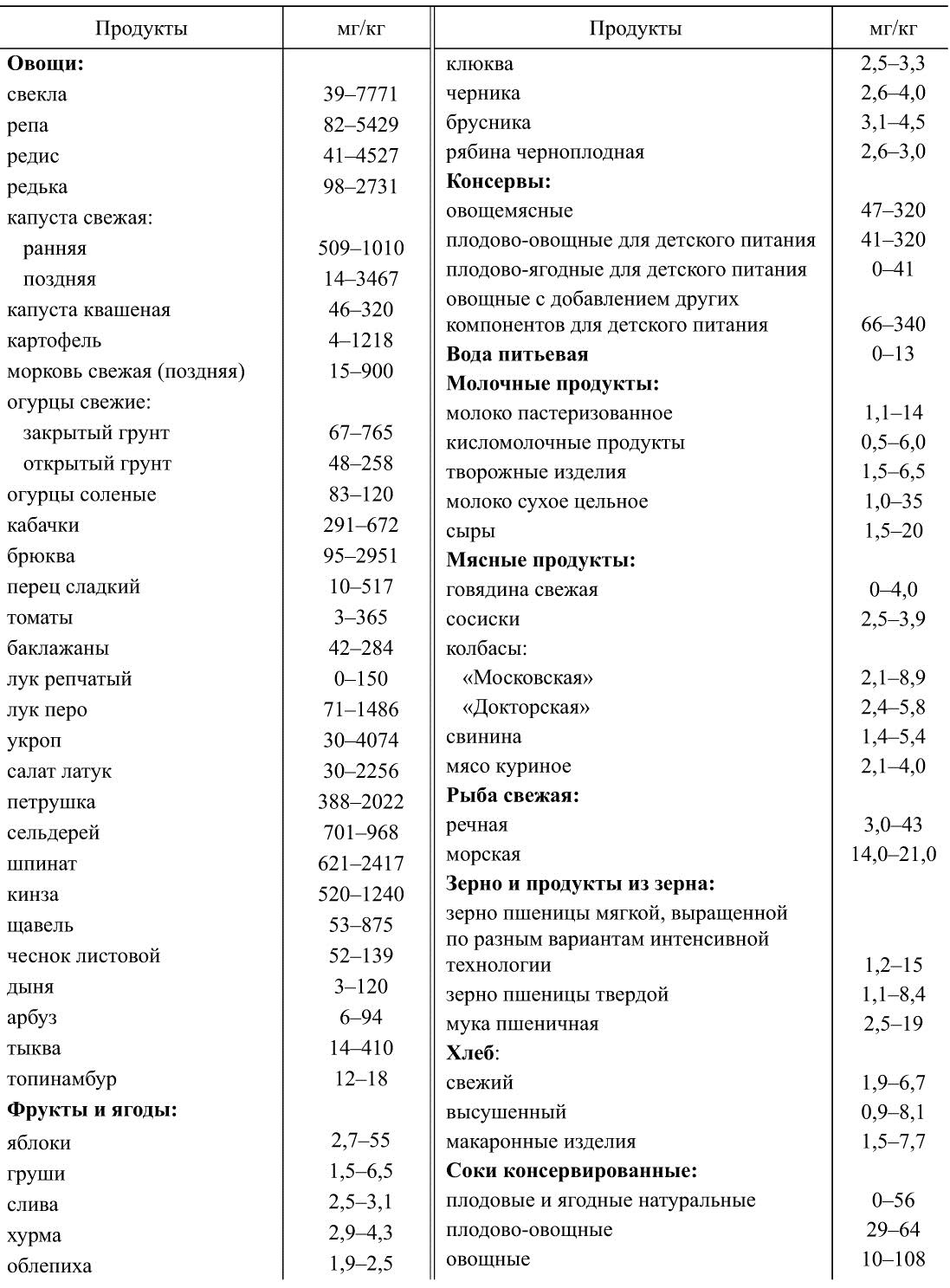
Таблица 36
Содержание нитритов в продовольственном сырье и пищевых продуктах (в пересчете на нитрит-ион)
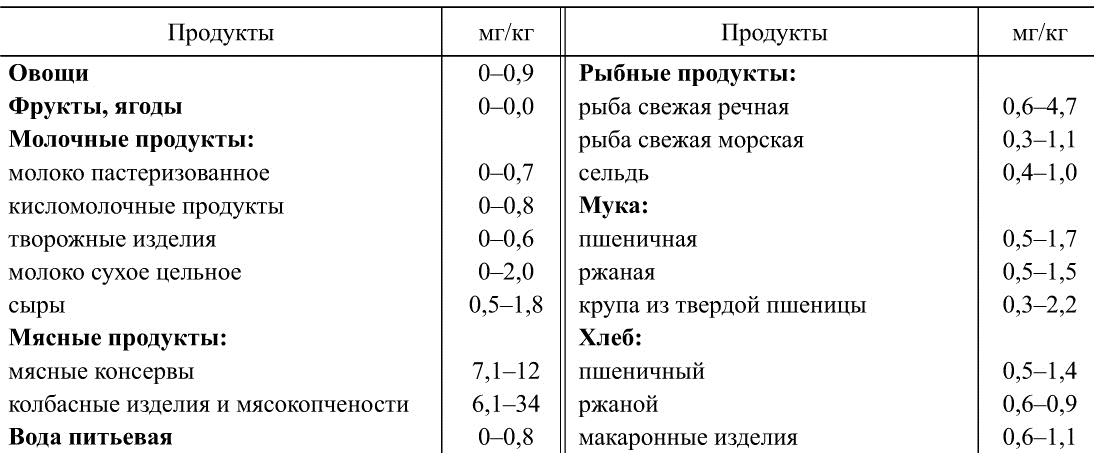
Согласно данным ФАО/ВОЗ, ДСД нитратов составляет 5 мг/кг массы тела в расчете на нитрат-ион. Мишенью действия больших доз нитратов являются ядра гепатоцитов и нуклеиновый обмен, что объясняет преимущественно эмбриотоксическое действие этих соединений.
НОРМИРОВАНИЕ НИТРАТОВ,
НИТРИТОВ КАК ПИЩЕВЫХ ДОБАВОК
Осуществляется в связи с их использованием в производстве некоторых продуктов питания. Содержание нитритов в пищевых продуктах допускается до 50 мг/кг, в солонине из говядины и баранины – до 200 мг/кг, в экспортируемых – до 30 мг/кг. Для обеспечения указанных нормативов нитриты используют в следующих количествах: засолка говядины, баранины и конины – 0,10-0,12 % от массы рассола; для свинины – 0,06-0,08 %, колбасных изделий – 0,003-0,005 % от массы мяса.
Нитрит натрия или калия используется в качестве консерванта сыра и брынзы – 300 мг на 1 л молока.
ДОПУСТИМЫЕ КОНЦЕНТРАЦИИ
В РАЦИОНЕ И ПРОДУКТАХ ПИТАНИЯ
ДСД нитратов для человека составляет 300-325 мг. ПДК в питьевой воде – 45 мг/л, или 10 мг нитратного азота в 1 л. Если учитывать потребление питьевой воды в размере 2 л в сутки, то на долю ДСП через пищевые продукты приходится 210 мг нитратов (300 – 45 2 = 210).
Основным источником поступления нитратов в организм человека являются продукты растительного происхождения, в частности овощи (82-92 %) (табл. 37). Основные поставщики нитритов – мясные продукты, на долю которых приходится 53-60 % от общего поступления нитритов в организм человека.
Таблица 37
Допустимые уровни содержания нитратов в продуктах растительного происхождения
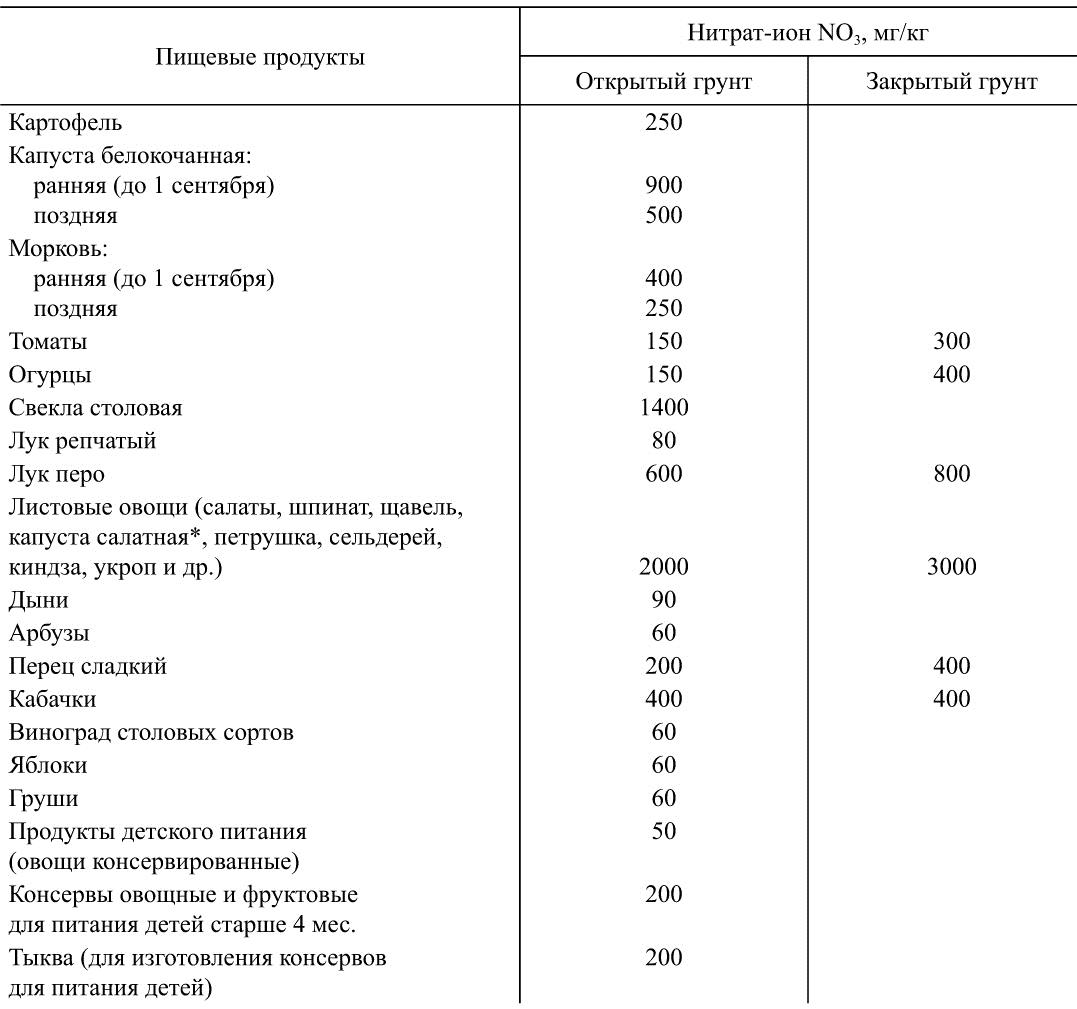
Источник: Санитарно-гигиенические нормы (№ 4619-88).
* Капуста салатных сортов, поставляемая по общероссийскому фонду до 1 июня.
Согласно рекомендациям ВОЗ, детей грудного возраста до 6 мес. не следует кормить продуктами с содержанием нитратов более 10 мг/кг, нитритов – более 0,05 мг/кг, поить питьевой водой с концентрацией нитратов более 1 мг/л, нитритов – более 0,005 мг/л.
Важное значение для снижения уровня загрязнения пищевых продуктов нитратами и нитритами имеет квалифицированная работа агрохимической и ветеринарной служб, соблюдение имеющихся правил и ведомственных документов.
НИТРОЗОСОЕДИНЕНИЯ (НС)
В настоящее время на живых организмах испытано более 300 нитрозосоединений, содержащихся в окружающей среде. Все они обладают канцерогенными, мутагенными, тератогенными и эмбриотоксическими свойствами. Канцерогенное действие этих соединений является определяющим.
Таблица 38
Максимальное содержание НДМА, НДЭА, НПиР, НПиП
в отечественных пищевых продуктах и продовольственном сырье

Источники: Рубенчик Б. Л. Питание, канцерогены и рак. Киев: Наук. думка, 1983; Жукова Г. Ф. Содержание N-нитрозоаминов в отечественных пищевых продуктах // Вопр. питания, 1988. № 6. С. 55–59.
Общей для НС является нитрозогруппа (N–N=O), к которой могут присоединяться различные радикалы: алкильный, арильный, алициклический и др., включая эфирные, ароматические амидогруппы и т. д.
Таблица 39
Допустимые уровни содержания N-нитрозаминов в продовольственном сырье и пищевых продуктах
(суммарное содержание N-нитрозодиметиламина и N-нитрозодиэтиламина)
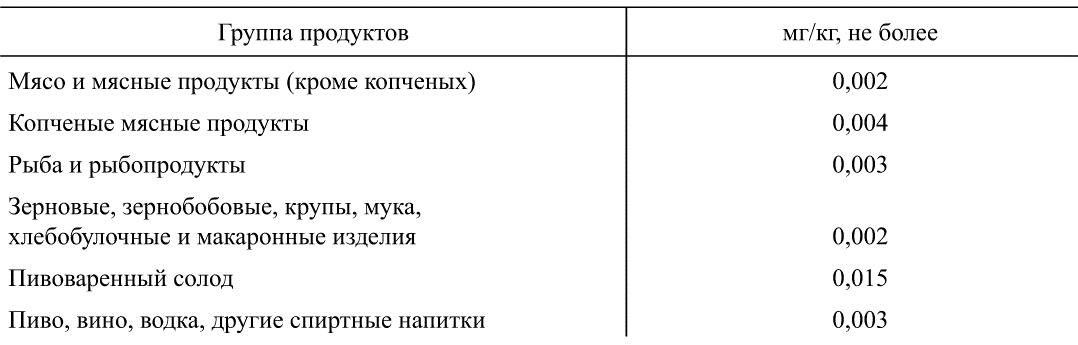
В общей схеме экзогенного воздействия на человека нитрозосоединений основное место отводится пищевым продуктам, что обусловлено широким применением в технологии их производства нитритов и коптильного дыма, содержащего окислы азота. Нитрит и оксиды азота обладают способностью легко нитрозировать вторичные и третичные амины пищевых продуктов с образованием нитрозосоединений.
НС могут образовываться в результате технологической обработки сельскохозяйственного сырья и полуфабрикатов, варки, жарения, соления, длительного хранения. При этом чем интенсивнее термическая обработка и длительнее хранение пищевых продуктов, тем больше вероятность образования в них НС.
В свежих продуктах НС содержатся в незначительных количествах, за исключением случаев, когда эти продукты изготовлены с нарушением технологических режимов и из сырья с высоким исходным уровнем предшественников реакций нитрозирования.
Нитраты и нитриты, содержащиеся в пищевых продуктах, являются предшественниками для эндогенного синтеза нитрозоаминов в организме человека.
Наибольшее распространение получили следующие нитрозосоединения: N-нитрозодиметиламин (НДМА), N-нитрозодиэтиламин (НДЭА), N-нитрозодипропиламин (НДПА), N-нитрозодибутиламин (НДБА), N-нитрозопиперидин (НПиП), N-нитрозопирролидин (НПиР).
Нитрозодиметиламин (НДМА) – основной канцероген, порождающий онкологические заболевания. Как и многие химические вещества в процессе синтеза, НДМА приобретает новые свойства и воздействует на человека как канцерогенный (злокачественные образования, 132 формы), эмбриотоксичный (поражение эмбриона), тератогенный (врожденные уродства) и мутагенный (нарушает генную структуру клетки, ДНК, и изменяет наследственность) фактор.
В настоящее время в США, Канаде и других развитых странах НДМА не используется в производстве или коммерции.
Содержание нитрозосоединений в отдельных группах пищевых продуктов представлено в табл. 38 (данные 1988 г.). В настоящее время картина загрязнения пищевой продукции остается практически прежней.
С суточным рационом человек получает ориентировочно 1 мкг НС, с питьевой водой – 0,01 мкг, с вдыхаемым воздухом – 0,3 мкг. В зависимости от степени загрязнения объектов окружающей среды эти цифры могут существенно колебаться. Половину всех НС человек получает с солено-копчеными продуктами. Допустимые уровни содержания НС в пищевых продуктах даны в табл. 39.







