Признаки, сгруппированные в этой главе, разделяют на микро- и макроморфологические, поскольку первые изучают с помощью микроскопа, а вторые – визуально.
Микроморфология включает признаки, характеризующие отдельные вегетативные клетки (форма, размеры), а также способы вегетативного или бесполого размножения и образуемые при этом структуры.
Макроморфология объединяет культуральные признаки, характеризующие рост культуры на плотных (сплошной рост по штриху, в виде изолированной и гигантской колонии) или в жидких средах.
2.1. ХАРАКТЕРИСТИКА ВЕГЕТАТИВНЫХ КЛЕТОК
Клетки дрожжей бывают круглые, овальные, яйцевидные, цилиндрические, треугольные, апикулятные (лимоновидные), колбовидные, стреловидные и серповидные. В некоторых случаях форма клетки бывает настолько характерна, что она может служить опознавательным признаком рода. Например, треугольные клетки образуются у Trigonopsis, серповидные – у Selenotila, грушевидные и колбовидные – у Schizoblastosporion, стреловидные – у Brettanomices.
У дрожжей не со столь характерной формой клеток в качестве вспомогательных признаков можно использовать, например, такие, как образование капсул и внутрицитоплазматических включений, представляющих собой резервные вещества разного химического состава. Скапливаясь в больших количествах, они придают клеткам весьма характерный вид.
Капсулы на клетках дрожжей различаются как по размерам, так и по форме. Толщина их варьирует от едва заметного слоя, обнаруживаемого только под электронным микроскопом (микрокапсула), до размеров, в несколько раз превышающих диаметр самой клетки. Капсульный материал обычно равномерно покрывает клетку, как это бывает у круглых клеток; у штаммов с овальными клетками он более обилен по полюсам. Следует, однако, помнить, что такие признаки, как наличие капсулы или включений, в очень большой степени зависят от штамма, условий культивирования и возраста культуры. Поэтому они имеют в диагностической практике лишь второстепенное значение.
Размеры «взрослых» дрожжевых клеток варьируют у разных видов от 1,5–2,0 до 10 мкм по ширине и достигают 20 мкм и более в длину у продолговатых. Мелкими клетками характеризуются, например, виды Pichia и Hansenula со шляповидными спорами и апикулятные дрожжи родов Hanseniaspora и Kloeckera. Крупные клетки имеют сахаромицеты, липомицеты, дрожжи с лимоновидными клетками родов Nadsonia, Saccharomycodes и Wickerhamia.
Форму и размеры клеток описывают и определяют в культурах разного возраста на плотных и жидких средах:
- солодовое сусло концентрацией 8–10% СВ;
- сусло-агар: к среде 1 добавляют 2% агара;
- глюкозопептонная жидкая среда;
- глюкозопептонный агар;
- морфологический агар.
Синтетические среды имеют то преимущество перед сусловыми, что они стандартны по составу и дают более стабильные и потому сравнимые результаты. Поэтому для составления стандартного описания видов лучше пользоваться морфологическим агаром.
Первый просмотр и измерение производят в двух-трехсуточных культурах, выращенных при 25–30°С. В особых случаях, когда дрожжи растут очень медленно, первое описание делают позже – через одну-две недели инкубации. Затем культуры оставляют при комнатной температуре (17–18°С) и еще раз описывают через четыре недели.
При определении размеров измеряют микрометром длину и ширину не менее чем у 20 клеток и указывают крайние значения. Для измерения лучше использовать культуры на жидких средах.
Капсулы выявляют на клетках из молодых и старых культур с плотных сред. Препараты клеток (без фиксации) готовят методом негативного окрашивания черной тушью. Для этого петлю с культурой смешивают на предметном стекле с каплей туши и слегка размазывают краем покровного стекла, держа его под углом 45°, а затем накрывают этим стеклом. Тушь можно заготовить впрок. Ее разбавляют в два раза, центрифугируют, супернатант стерилизуют и хранят в запаянных ампулах. Хорошие результаты получаются с тушью, приготовленной по методу Литтмана.
Дрожжи размножаются вегетативно путем почкования, деления или почкующегося деления.
При почковании на поверхности клетки образуется маленькое выпячивание – почка, которая увеличивается почти до размеров материнской клетки и отделяется от нее, оставляя на месте бывшего прикрепления почковый шрам или рубец в виде кольцеобразного выступа (рис. 1).
Если одновременно или последовательно образующиеся почки формируются на разных сторонах материнской клетки, то такое почкование называют множественным или многосторонним соответственно.
Почки могут закладываться и на широком основании, которое сужается к моменту отделения почки; иногда же, наоборот, почки образуются на узком и довольно заметном выросте. Для рода Sterigmatomyces характерен своеобразный процесс образования почек на длинных выростах, имитирующих стеригмы.
Полярное образование дочерних клеток, начинающееся с формирования почки на широком основании и заканчивающееся появлением четко заметной даже в световом микроскопе септы в районе перешейка, носит название почкующегося деления.
Если при почковании клетки не разъединяются, а продолжают образовывать все новые и новые почки, то в конце концов формируются структуры ложных гиф, из которых складывается псевдомицелий. Он бывает примитивным, если состоит из продолговатых клеток приблизительно одинакового размера, или же хорошо развитый, если дифференцируется на длинные клетки псевдогиф и окружающие их в характерном порядке (кучками, мутовками, поодиночке) клетки другой формы, именуемые бластоспорами.
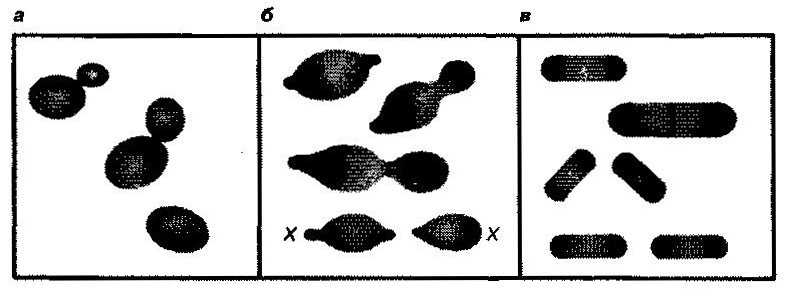
Рис.1
Вегетативное размножение дрожжей:
а – мультилатеральное почкование (как у Saccharomyces); б – биполярное почкование (как у Hanseniaspora). При следующей генерации две помеченные клетки будут образовывать почку с конца X; в – бинарное деление (как у Schizosaccharomyces).
Если дрожжи размножаются делением, то при образовании нитевидных структур они формируют истинный мицелий. При распаде такого мицелия на отдельные клетки последние носят название артроспор. На плотной среде они часто располагаются характерным зигзагом.
Эндоспоры – внутриклеточные бесполые споры – появляются в неопределенном числе в клетках гиф в старых культурах. Клетки при этом иногда заметно раздуваются.
Способы вегетативного размножения наблюдают одновременно с описанием микроморфологин дрожжей на тех же средах в культурах 2– 3-суточного возраста.