20.1. ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА В ПРЕССОВАННЫХ ДРОЖЖАХ
В товарных дрожжах обычно содержится 1,65–1,8% азота, в засевных – 2,0–2,2%, а в маточных – 2,2–2,4% азота.
Анализу подвергают пробы на любом этапе технологического процесса от каждого затора или от каждой партии дрожжей.
Общий азот в прессованных дрожжах определяют по методу Кьельдаля.
Около 4 г прессованных дрожжей отвешивают в бюксе на аналитических весах с точностью до четвертого знака и переносят в колбу Кьельдаля. Остаток дрожжей в бюксе взвешивают и по разности определяют вес взятой навески. В колбу наливают 20 см3 концентрированной серной кислоты «ХЧ», помещают 2–3 крупинки селена или около 1 г сернокислой меди и около 10 г сернокислого калия. Если в дальнейшем в этой же навеске дрожжей определяют и фосфор, сжигание с медью производить нельзя. Содержимое колбы осторожно смешивают, слегка вращая колбу, и закрывают ее специальной стеклянной пробкой с расширением, неплотно вставляющейся в горло колбы.
Затем колбу ставят в наклонном положении в вытяжной шкаф на нагревательный прибор (плитку или газовую горелку). Сначала сжигание ведут при слабом нагревании, при этом происходит обугливание и выделение сернистого газа, затем, когда выделение газа станет более равномерным, нагревание усиливают. Когда жидкость перестанет пениться, обуглившиеся, но несгоревшие комочки вещества, приставшие к стенкам, осторожным помешиванием смывают в жидкость, которая постепенно становится совершенно прозрачной. Прозрачную жидкость нагревают еще 1–2 ч.
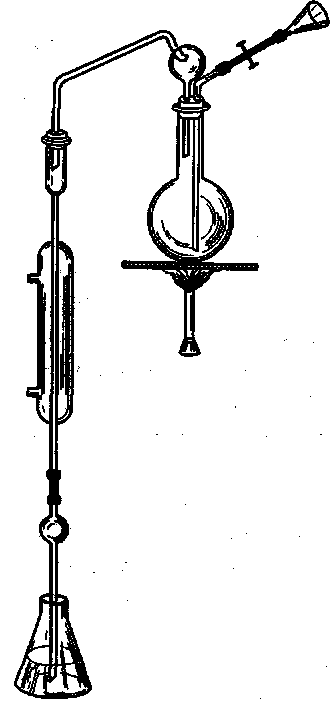
Рис. 39
Прибор для определения азота по Кьельдалю
После сжигания содержимое колбы Кьельдаля смешивают с небольшим количеством воды и переливают в мерную колбу емкостью 250 см3, споласкивают колбу Кьельдаля еще 2–3 раза и промывную воду сливают в ту же мерную колбу. Затем содержимое ее доводят водой до метки, хорошо перемешивают и переводят в колбу для отгона аммиака.
Перегонку производят или в специальном приборе, где можно одновременно проводить несколько определений, или в аппарате (рис. 39), который собирают следующим образом: круглодонную или плоскодонную колбу емкостью 1 л устанавливают на штатив, соединяют ее плотной резиновой пробкой с каплеуловителем, а затем с холодильником. В пробку, кроме трубки каплеуловителя, вставляют стеклянную трубку, соединенную каучуковой трубкой с небольшой воронкой диаметром 4–5 см; на каучуковой трубке имеется винтовой зажим.
К другому концу холодильника присоединяют стеклянную трубку с шарообразным расширением в верхней части, которую опускают почти до дна приемника. Приемником может служить обычная коническая колба емкостью 500 см3. Все части прибора должны быть плотно пригнаны. В приемник наливают 50 см3 0,1 Н раствора серной кислоты и 1–2 капли раствора метилрот и устанавливают его так, чтобы конец трубки с шарообразным расширением был погружен в кислоту.
Содержимое колбы Кьельдаля после охлаждения разбавляют дистиллированной водой небольшими порциями и сливают через воронку в колбу для отгонки. Колбу Кьельдаля ополаскивают несколько раз водой с таким расчетом, чтобы общий объем жидкости составлял около 400–500 см3. Колбу помещают на штатив и собирают аппарат, как было указано выше. Затем открывают винтовой зажим воронки и наливают 50–100 см3 33%-ного раствора едкой щелочи. Воронку смывают небольшим количеством дистиллированной воды, завинчивают зажим и содержимое колбы взбалтывают. Наличие в колбе для отгонки избытка щелочи устанавливают при помощи кусочка лакмусовой бумажки, брошенной в колбу. Лакмусовая бумажка синеет.
Колбу для отгонки подогревают горелкой и отгоняют аммиак с водяными парами до тех пор, пока капля отгона не перестанет вызывать посинения красной лакмусовой бумажки. Для этого достаточно отогнать из колбы около половины всей жидкости.
По окончании отгонки конец трубки, опущенный в кислоту, споласкивают водой в приемник и содержимое приемника титруют 0,1 Н раствором щелочи. Затем определяют количество миллилитров 0,1 Н раствора едкого натра, израсходованного на титрование серной кислоты, не связавшейся аммиаком, после чего производят расчет. Количество связанной кислоты соответствует выделившемуся аммиаку. 1 см3 0,1 Н щелочи соответствует 1,40 мг азота.
Если параллельно с определением азота производят определение фосфора, то из мерной колбы сначала отбирают 50 мл для этого определения, а остальной раствор переводят в колбу для отгона аммиака.
Содержание азота (N) в процентах вычисляют по следующей формуле:
![]()
где a – количество 0,1 Н раствора серной кислоты, налитой в приемник, в см3 (1 см3 0,1 Н раствора серной кислоты соответствует 0,0014 г азота); б – количество 0,1 Н раствора щелочи, затраченное на титрование, в см3; р – навеска дрожжей в г.
Общее количество белковых веществ вычисляют путем умножения количества общего азота на коэффициент 6,25.
Пример. Для анализа взято 4,8200 г дрожжей. Для определения фосфора отобрана 1/5 часть, что составляет 4,82 : 5 = 0,964 г; для определения азота взято 4,8200 – 0,964 = 3,8560 г. В приемник налито 75 см3 0,1 Н серной кислоты, на титрование оставшейся свободной кислоты затрачено 22,4 см3 0,1 Н раствора едкого натра. Аммиаком связано
75 – 22,4 = 52,6 см3 кислоты. Следовательно, содержание азота в дрожжах составит
![]()
20.2. ОПРЕДЕЛЕНИЕ ФОСФОРНОГО АНГИДРИДА В ДРОЖЖАХ
В прессованных дрожжах содержится от 0,7 до 1,4% Р2O5. Содержание фосфорного ангидрида в дрожжах определяют колориметрическим методом Бриггса или при помощи фотоэлектроколориметра.
Визуальный метод. Принцип метода основан на образовании фосфорномолибденовой кислоты и ее восстановлении гидрохиноном и Na2SO4 с образованием устойчивой синей окраски. Интенсивность окраски возрастает пропорционально количеству неорганического фосфора в испытуемой пробе.
Навеску прессованных дрожжей около 1 г помещают в колбу Кьельдаля и сжигают ее так же, как при определении общего азота. После сжигания содержимое колбы переводят в мерную колбу емкостью 100 см3. Колбу Кьельдаля несколько раз ополаскивают водой, которую также сливают в мерную колбу, затем содержимое колбы доводят водой приблизительно до 50 см3, нейтрализуют 33%-ным раствором едкого натра и доливают водой до метки, т. е. до объема 100 см3, и хорошо перемешивают. Из приготовленного таким образом раствора отбирают 1 см3 в пробирку высотой 70 мм и диаметром 15 мм. Одновременно в семи других пробирках такого же размера готовят стандартный ряд с определенными, все увеличивающимися концентрациями фосфора: 0,01; 0,02; 0,03; 0,04; 0,05; 0,06; 0,07 мг фосфора в 1 см3.
В первую из семи пробирок наливают 0,1 см3 стандартного раствора КН2РO4, что соответствует 0,01 мг фосфора; во вторую – 0,2 см3, т. е. 0,02 мг фосфора; в третью – 0,3; в четвертую – 0,4; в пятую – 0,5; в шестую – 0,6; в седьмую– 0,7 см3. Затем в первую пробирку доливают 0,9 см3 воды, во вторую – 0,8, в третью – 0,7, в четвертую – 0,6, в пятую – 0,5, в шестую – 0,4, в седьмую – 0,3. Таким образом, в каждой из семи пробирок объем жидкости равняется 1 см3.
Затем в каждую из восьми пробирок наливают по 1 см3 молибденового раствора, по 1 см3 раствора гидрохинона и по 1 см3 раствора безводного сульфита. После взбалтывания содержимое пробирок окрашивается в различные по интенсивности оттенки синего цвета – от светло-синего до темно-синего. Пробирки оставляют стоять на 20 мин, после чего сравнивают окраску пробирки с испытуемой жидкостью с окраской каждой из семи пробирок, содержащих стандартный раствор. Содержание фосфора в анализируемых дрожжах рассчитывают по формуле
![]()
где A – содержание Р2O5 в прессованных дрожжах в %; а – содержание фосфора в пробирке с испытуемым веществом (по стандартному ряду); б – разведение; В – навеска вещества (в пересчете на 75% влаги); 2,29 – коэффициент перевода Р в Р2O5 (частное от деления молекулярного веса Р2O5 на молекулярный вес фосфора – 142 : 62 = 2,29); 100 – пересчет на проценты; 1000 – перевод мг в г.
Пример. Цвет пробирки с испытуемым раствором соответствует цвету пробирки стандартного ряда, содержащей 0,04 мг фосфора. Подставляем наши данные в формулу и производим расчет содержания Р2O5 в прессованных дрожжах:
![]()
Растворы для определения фосфора по методу Бриггса.
- 5%-ный молибденовый раствор. 25 г молибденовокислого аммония растворяют в 300 см3 дистиллированной воды, к полученному раствору добавляют 75 см3 концентрированной серной кислоты, разбавленной 120 см3 воды; общий объем раствора доводят водой до 500 см3.
- Свежеприготовленный 1%-ный раствор гидрохинона. К 100 см3 раствора добавляют каплю концентрированной серной кислоты для предотвращения окисления.
- 20%-ный раствор безводного сульфита (Nа2SO3). Вследствие окисления сульфитный раствор портится при долгом хранении, поэтому пользуются свежеприготовленным раствором.
- Стандартный раствор кислого фосфорнокислого калия. Готовят из чистой соли КН2РО4, которую предварительно измельчают и высушивают в эксикаторе в течение нескольких дней. 4,394 г соли растворяют в дистиллированной воде (1 дм3) и добавляют несколько капель хлороформа как антисептика. 1 см3 раствора содержит 1 мг фосфора. 100 см3 этого раствора разбавляют водой до 1 дм3 и получают раствор, в 1 см3 которого содержится 0,1 мг фосфора.
Фотоэлектроколориметрический метод. В модельных растворах стандартного ряда пробирок определяют оптическую плотность с помощью прибора ФЭК и строят калибровочный график. На оси абсцисс откладывают количество фосфора, а на оси ординат – оптическую плотность. Для данной шкалы стандартного ряда пробирок график будет постоянным.
Определив на приборе ФЭК оптическую плотность пробирки с испытуемым раствором, по графику находят соответствующее ей содержание фосфора в пробирке.
20.3. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ЗОЛЫ
В прессованных дрожжах содержание золы обычно колеблется от 1,6 до 2%. В пересчете на прессованные дрожжи с содержанием 75% влаги оно не должно быть выше 2,5%, а на сухое вещество дрожжей – не более 10%.
Около 2 г прессованных дрожжей отвешивают на аналитических весах с точностью до четвертого знака в предварительно прокаленном платиновом или фарфоровом тигле. Навеску предварительно подсушивают при температуре 70–80°С; когда консистенция дрожжей станет такой, что можно не опасаться разбрызгивания, добавляют 8–10 капель серной кислоты удельным весом 1,84, размешивают оплавленной стеклянной палочкой, вытирают палочку маленьким кусочком фильтровальной бумаги, который также бросают в чашку и, держа чашку щипцами, осторожно нагревают на небольшом пламени горелки под тягой. Когда масса перестанет пениться и выделение паров и газов прекратится, ее окончательно сжигают и прокаливают до постоянного веса в муфеле при слабом калении или на горелке, при этом доводят платиновую чашку или тигель до слабо-красного каления.
Сжигание навески считается законченным, когда вся масса превратится в белый или розовый порошок, не содержащий черных частиц несгоревшего вещества. Затем чашку или тигель переносят в эксикатор, охлаждают и взвешивают.
Полученный вес сернокислой золы для перевода на условную углекислую золу умножают на коэффициент 0,9 и пересчитывают на 100 г дрожжей.
П р и м е р. Вес (в г) равен:
тигля с навеской дрожжей.................. 18,3100
тигля прокаленного пустого .............. 15,5421
навески дрожжей..................................... 2,7683
тигля с золой............................................ 15,7436
золы.............................................................. 0,2015
Вес углекислой золы (в г) составит 0,2015 · 0,9 = 0,18135.
Содержание золы (в %) равно
![]()
20.4. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ГЛУТАТИОНА
Метод основан на том, что в кислой среде в присутствии йодистого калия восстановленная форма глутатиона под действием КJО3 переходит в окисленную.
Глутатион в восстановленной форме содержит сульфгидрильную группу (SН) и является активатором протеолиза; в сахаромицетах его 0,6–0,8, что в 4–5 раз больше, чем в несахаромицетах – 0,15–0,1. Поэтому содержание глутатиона может служить относительным показателем степени загрязненности прессованных дрожжей посторонними дрожжевыми грибами. Но, что не менее важно, метод может быть использован как косвенный показатель функциональной полноценности клеточной стенки.
Определение глутатиона – йодредуцирующих веществ – производят с помощью йодноватокислого калия и выражают в мл 0,001 Н раствора КJО3, пошедшего на титрование 1 г прессованных дрожжей.
Ход определения. 10 г исследуемых дрожжей помещают в колбу, постепенно приливают 95 см3 дистиллированной воды и размешивают; через 5 мин добавляют 5 см3 молярного раствора сульфосалициловой кислоты (25 г на 100 см3 дистиллированной воды). Смесь тщательно встряхивают, фильтруют через сухой обеззоленный фильтр и из фильтрата берут 10 см3 в небольшую колбу. В ту же колбу добавляют 2,5 см3 4%-ной сульфосалициловой кислоты, 2,5 см3 5%-ного раствора химически чистого КJ (приготовляемого ежедневно и проверенного на отсутствие следов йода), 10 капель 1%-ного раствора крахмала (в воде или лучше в насыщенном растворе КСl или NaCl), осторожно оттитровывают из микробюретки 0,001 Н раствором КJО3 до первого изменения окраски.
Титрование производят при температуре растворов, не превышающей 20°С. Таким же путем ставят и контрольное определение, заменяя только испытуемый раствор 10 см3 дистиллированной воды и вычитая полученные цифры из результатов основного опыта. Полученные результаты выражают в см3 0,001 Н КJО3 на 1 г прессованных дрожжей.
Общий запас восстановленного глутатиона определяют после 5-минутного кипячения дрожжей с водой с применением той же методики.
Растворы для определения глутатиона.
- Молярный раствор сульфосалициловой кислоты. 25 г на 100 см3 дистиллированной воды.
- 24%-ный раствор сульфосалициловой кислоты. 18 см3 молярного раствора разбавляют до 100 см3 дистиллированной водой.
- 0,001 Н раствор йодноватокислого калия. 0,1783 г перекристаллизованного химически чистого КJО3 растворяют в мерной колбе на 1 дм3, откуда берут 20 см3 раствора, прибавляют 9 см3 молярного раствора сульфосалициловой кислоты и доводят дистиллированной водой до 100 см3 в мерной колбе. Этот разбавленный раствор КJО3 следует приготовлять каждую пятидневку и хранить при пониженной температуре. 8,5 г КJО3 растворяют в 100 см3 дистиллированной воды, содержимое фильтруют. Для кристаллизации соли фильтрат помещают в холодильник на ночь, осадок отфильтровывают и высушивают между листами фильтровальной бумаги. Полученную соль хранят в темной стеклянной банке с притертой пробкой.







